作者,Evil Genius
我们下周拉群,培训2025番外--linux、R、python培训 https://mp.weixin.qq.com/s/8E1vYJMNhe5m0DXieBHfzA, 做生信8年了,我会针对单细胞空间常用的基础内容进行培训,让大家掌握基础的Linux、R、和python,让大家分析单细胞空间外显子,基础的内容不会成为卡点,看到想分析的内容,可以通过思想把代码构思并且实现出来。
https://mp.weixin.qq.com/s/8E1vYJMNhe5m0DXieBHfzA, 做生信8年了,我会针对单细胞空间常用的基础内容进行培训,让大家掌握基础的Linux、R、和python,让大家分析单细胞空间外显子,基础的内容不会成为卡点,看到想分析的内容,可以通过思想把代码构思并且实现出来。
我呢,就是尽力培训,中间穿插一些单细胞空间的分析思路,以及在写代码的时候需要注意的内容和格式,如果有人想从事生信分析岗位,这种基础是必须的。
经历了这么多,真的感觉到,没有人容易,但是大家也都在努力的前进。
生信职场或者科研的第一课,就是基础代码能力,有了这个1,后面无数的0才有意义。
今天我们分享文献,清华大学发的文章。

知识积累
肾脏肿瘤是第三大常见的泌尿系统恶性肿瘤,占所有成人癌症的2% ~ 3%。其中超过90%为起源于肾小管上皮细胞的肾细胞癌(RCC),而透明细胞肾细胞癌是最主要的亚型(约75%)。在RCC中,肿瘤可能侵入肾静脉或下腔静脉形成瘤栓(TT),约有4%~10%的RCC患者会受此影响。瘤栓的存在显著影响RCC的临床分期、手术策略和预后。既往研究已证实,瘤栓是一个强烈关联更差生存率和更高复发风险的不良预后因素。此外,高级别的瘤栓增加了手术的复杂性和风险,进而导致更高的围手术期并发症(34%)和死亡率(10%)。
最近的基因组研究发现,瘤栓很可能起源于原发肿瘤的亚克隆,且仅带有极少的额外突变。值得注意的是,来自伴瘤栓患者的原发肿瘤,其突变负荷和基因组不稳定性(尤其是在BAP1、SETD2等染色质重塑基因中)显著高于不伴瘤栓患者的原发肿瘤。
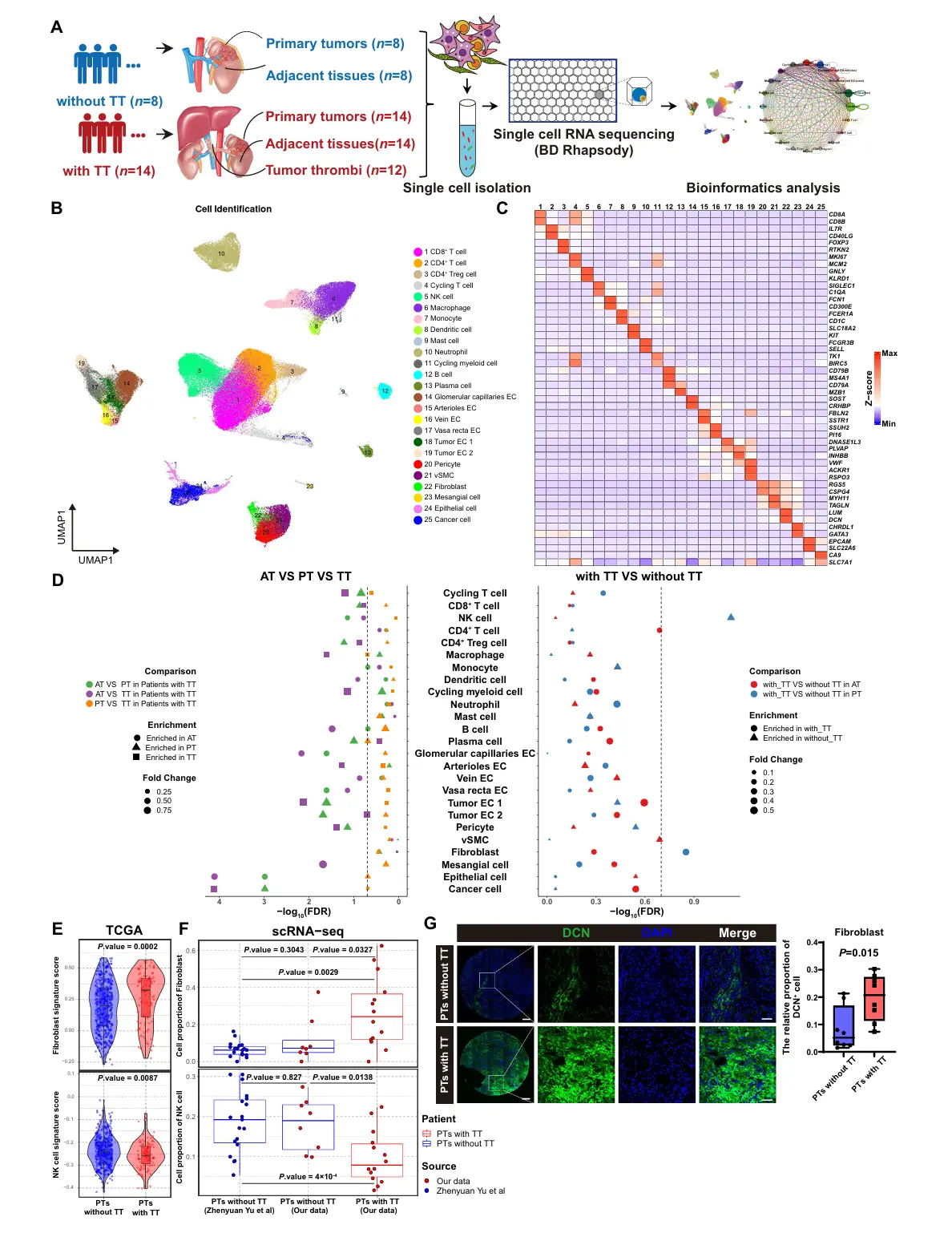
结果1、单细胞图谱构建
瘤栓相关的肿瘤微环境变化
首先在同一TT患者体内比较了不同组织区域(AT、PT、TT)的细胞组成。结果显示,AT与肿瘤(PT/TT)之间存在显著差异:AT富集正常上皮细胞和NK/B细胞等,而肿瘤区域则富集癌细胞、肿瘤内皮细胞和调节性T细胞、巨噬细胞等。然而,PT与TT之间的细胞比例无统计学差异。
比较了伴TT与不伴TT患者在其原发肿瘤(PT) 中的细胞组成。关键发现是:与不伴TT的患者相比,伴TT患者的PT中具有更高比例的成纤维细胞和更低比例的自然杀伤(NK)细胞。
细胞通讯分析进一步显示,在伴TT的RCC肿瘤微环境中,成纤维细胞拥有最活跃的细胞间相互作用,提示其在协调细胞间通讯中可能扮演核心角色。
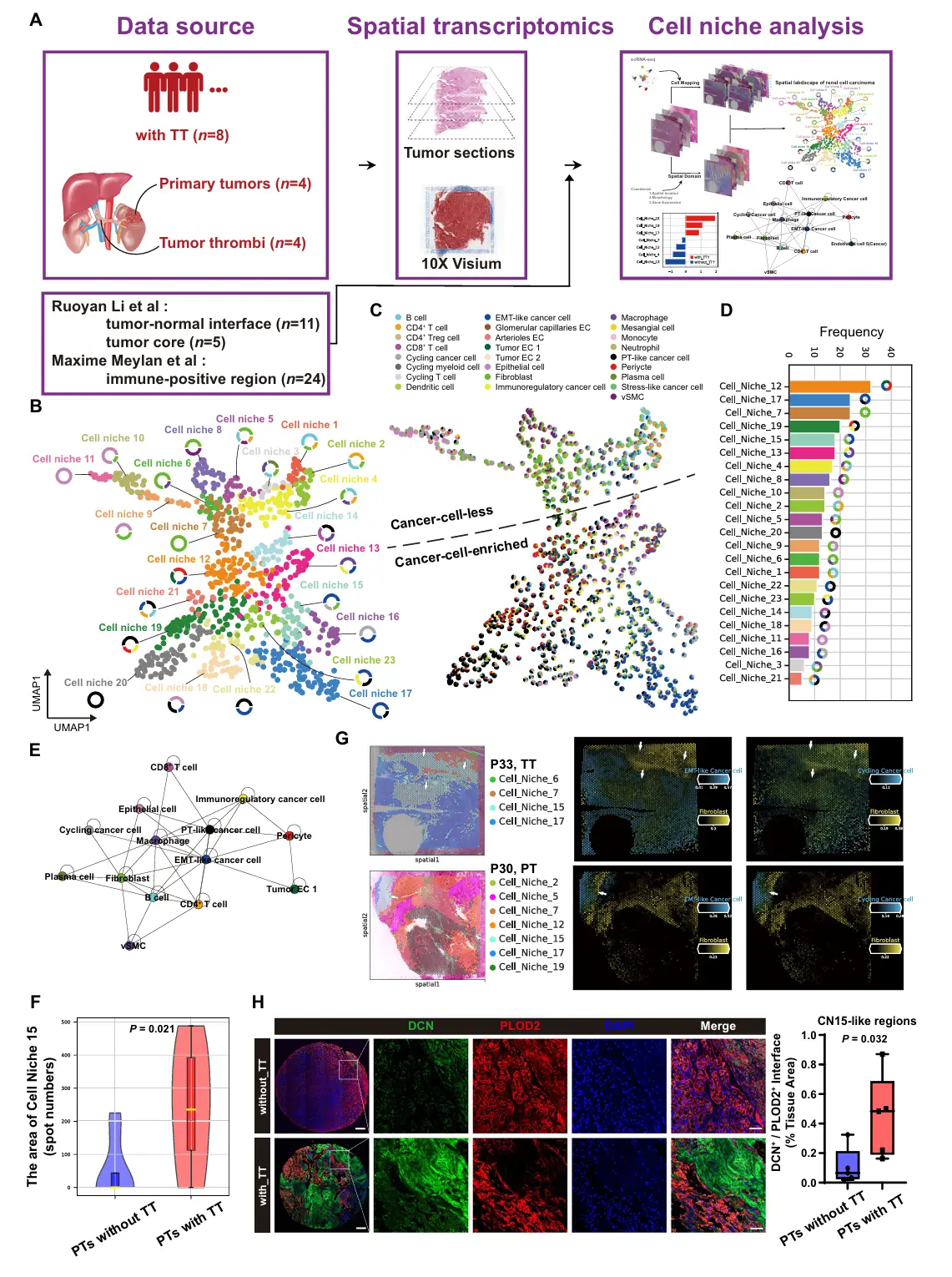
结果2、肾细胞癌的空间组织结构
细胞在肿瘤内的空间位置被揭示与其功能和状态密切相关。
10X Visium数据,包括肿瘤-正常组织交界区、肿瘤核心区和免疫阳性区的样本。
cell2location对每个空间转录组样本进行了细胞类型的空间定位。同时,利用stLearn(整合空间位置、形态学和基因表达)鉴定了每个空间转录组样本内的空间域。
通过整合所有空间转录组样本的空间域,我们在RCC的TME内鉴定出23个不同的CNs,并将其分类为无癌细胞niche(CN1-11)或富集癌细胞niche(CN12-23)
发现关键细胞niche CN15:
组成特征: CN15是一个由EMT样癌细胞、周期中癌细胞和成纤维细胞共同富集的空间单元。
核心发现: CN15在伴瘤栓(TT)的RCC患者的原发肿瘤(PT)中显著扩张。这一发现通过了多重免疫荧光等独立实验方法的验证,且在排除多种混杂因素后依然成立。
成纤维细胞的核心作用:
成纤维细胞相关的细胞niche(CN7, CN15)出现频率很高,提示其在RCC中作用广泛。
空间网络分析显示,成纤维细胞能与B细胞、巨噬细胞、血管平滑肌细胞、上皮细胞以及癌细胞(形成CN15) 等多种细胞相互作用,表明其功能异质性强,是TME中的关键“协调者”。
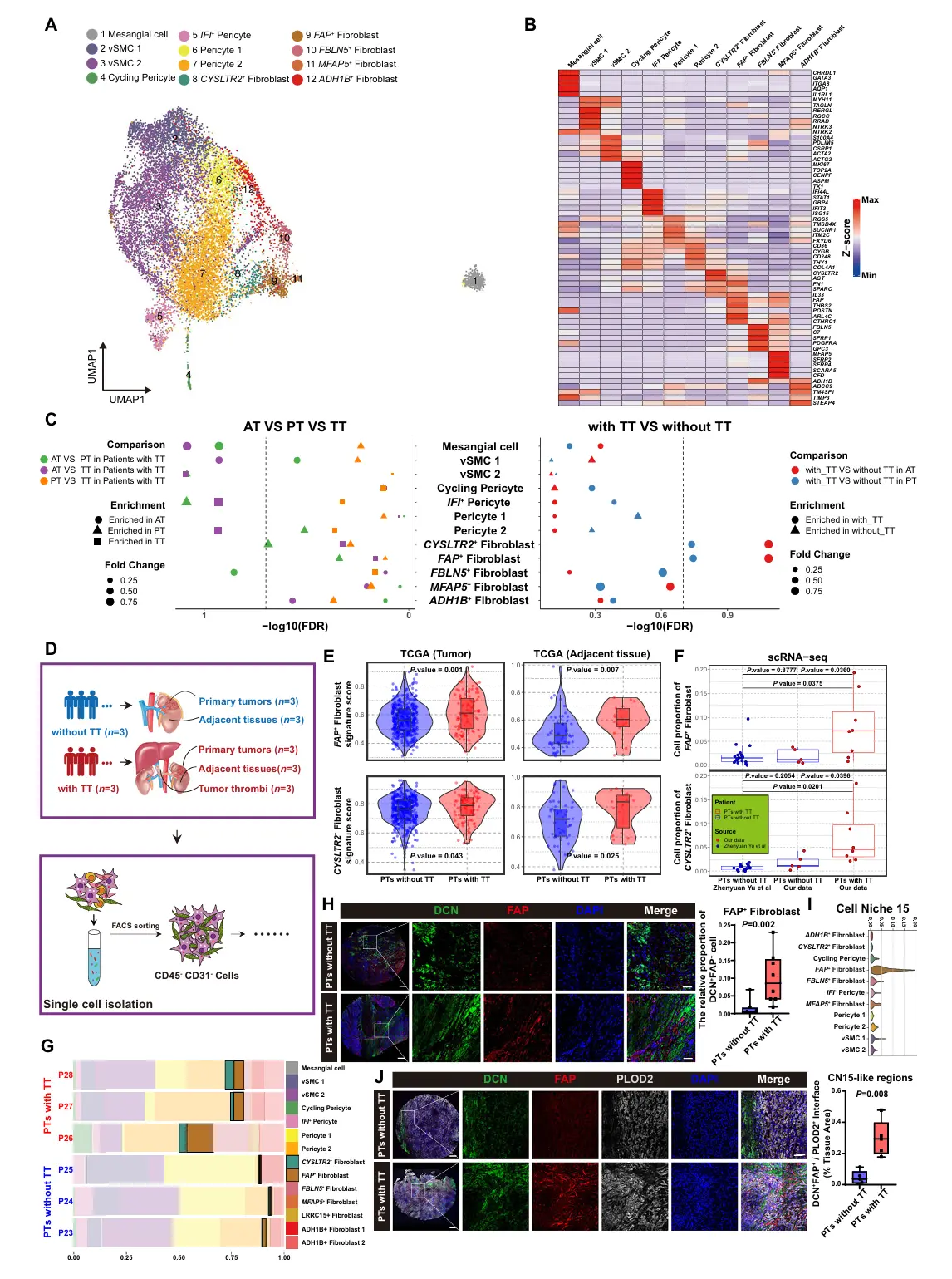
结果3、肾细胞癌发生与进展中的基质重塑
对成纤维细胞及其他间充质细胞进行了亚群分析,鉴定出12个间充质细胞亚群,包括2个血管平滑肌细胞(vSMC)亚群、4个周细胞亚群、5个成纤维细胞亚群和系膜细胞。
血管周围细胞(vSMC/周细胞)的状态改变:
分析发现,vSMC2和周细胞2亚群在肿瘤(PT/TT)中比例增加,而vSMC1主要存在于正常组织(AT)中。
vSMC2和周细胞2高表达与细胞外基质(ECM)重塑和干细胞特性相关的基因,表明在RCC肿瘤发生过程中发生了血管周围细胞状态的改变和潜在的血管重塑。
成纤维细胞亚群的特征与鉴定:
在五个成纤维细胞亚群中,FAP+ 成纤维细胞和CYSLTR2+ 成纤维细胞被鉴定为潜在的癌症相关成纤维细胞(CAFs)。
证据如下:
它们在肿瘤组织(PT)中显著富集。
在空间位置上,它们主要分布于肿瘤核心区和癌细胞富集的细胞niche(CNs)中。
它们无法被正常肾脏的间充质细胞标签所注释,表明它们是肿瘤演化过程中的重塑产物。
它们表达多种CAFs和肌成纤维细胞的标志物。
成纤维细胞与瘤栓(TT)的关键关联:
比较伴TT与不伴TT的患者发现,伴TT患者的原发肿瘤(PT)和甚至其癌旁组织(AT)中,FAP+ 和 CYSLTR2+ 成纤维细胞的比例都显著升高。这一发现在TCGA数据库、独立验证队列的多组学数据以及多重免疫荧光实验中均得到证实。
细胞互作分析显示,FAP+ 成纤维细胞在伴TT的RCC肿瘤微环境中拥有最活跃且高度激活的相互作用。
最关键的是,在伴TT患者中显著扩张的关键细胞niche CN15(富含EMT样癌细胞和成纤维细胞)中,其中的成纤维细胞几乎全部是FAP+ 成纤维细胞。
结果4、RCC中的周细胞-成纤维细胞转化:从周细胞2到CYSLTR2+成纤维细胞,再到FAP+成纤维细胞
发现细胞转化路径: 明确了一条清晰的细胞转化路径:肿瘤周细胞(Pericyte 2)→ CYSLTR2+ 成纤维细胞(过渡状态)→ FAP+ 成纤维细胞(终末状态)。该路径通过拟时序分析、RNA速率和空间转录组学等多重技术得到证实。
揭示转化在TT形成中的关键作用:
在伴TT的RCC患者中,这一周细胞-成纤维细胞转化过程被显著激活和加速。
肿瘤内皮细胞高表达的PDGFB通过PDGFRβ信号驱动了这一转化。
转化过程中的细胞(周细胞、过渡态和终末态)高表达促癌胶原基因,共同构成了促肿瘤微环境。
阐明核心转录调控机制:
CREB3L1:其活性和表达在转化过程中逐渐上调,是启动和维持FAP+ 成纤维细胞身份的关键促进因子。
MEF2C:其活性和表达在转化过程中逐渐下调,作为周细胞身份的"守护者",其抑制可能解除了对成纤维细胞程序的刹车,从而允许转化发生。

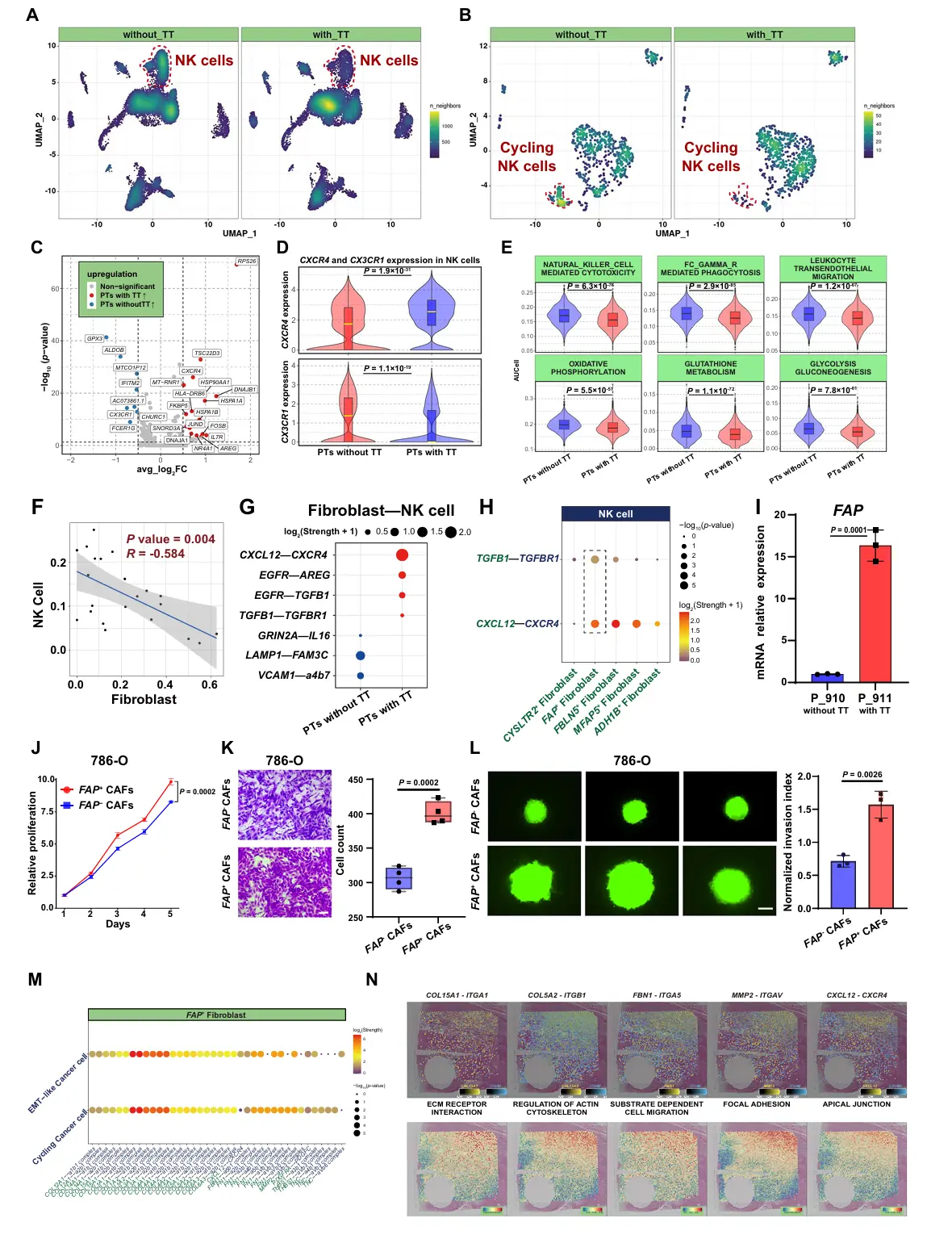
结果5、FAP+ 成纤维细胞介导NK细胞抑制并直接调控癌细胞促进瘤栓发展
FAP+ 成纤维细胞介导NK细胞抑制
现象: 在伴TT患者的PT中,NK细胞的比例和增殖能力(周期中的NK细胞)显著降低,功能受损(细胞毒性、迁移能力下降),且表现出更不成熟的基因特征(高表达CXCR4,低表达CX3CR1)。
机制:
相关性: 成纤维细胞的总比例与NK细胞的比例和细胞毒性呈显著负相关。
相互作用: 细胞通讯分析发现,在伴TT患者中,成纤维细胞(尤其是FAP+ 亚群)通过CXCL12-CXCR4和TGFB1-TGFBR1信号通路与NK细胞发生特异性相互作用。这两种信号分别可诱导NK细胞静息和抑制其代谢(糖酵解和氧化磷酸化),从而导致NK细胞功能失调。
核心角色: 回归模型显示,FAP+ 成纤维细胞是预测NK细胞减少的最强负相关因素之一。
2. FAP+ 成纤维细胞直接调控癌细胞(尤其是EMT样癌细胞)促进TT发展
功能验证: 体外实验证实,从RCC组织中分离出的FAP+ 成纤维细胞相较于FAP-成纤维细胞,能显著增强RCC细胞系的增殖、迁移和3D球体侵袭能力。
机制探索:
相互作用: FAP+ 成纤维细胞与EMT样癌细胞和周期中癌细胞通过ECM-整合素信号等发生强烈相互作用。
信号激活: 在伴TT患者的EMT样癌细胞中,整合素相关通路(如ECM-受体相互作用、细胞骨架调控、粘着斑等)的活性显著升高,表明ECM-整合素信号增强。
空间共定位: 在空间转录组数据中,在富含FAP+ 成纤维细胞和癌细胞的CN15 niche内及其边界,发现了COL15A1-ITGA3、MMP2-ITGAV/ITGB3、CXCL12-CXCR4等配体-受体对的共表达,且这些区域的整合素通路评分也更高,形成了促癌侵袭的协同微环境。
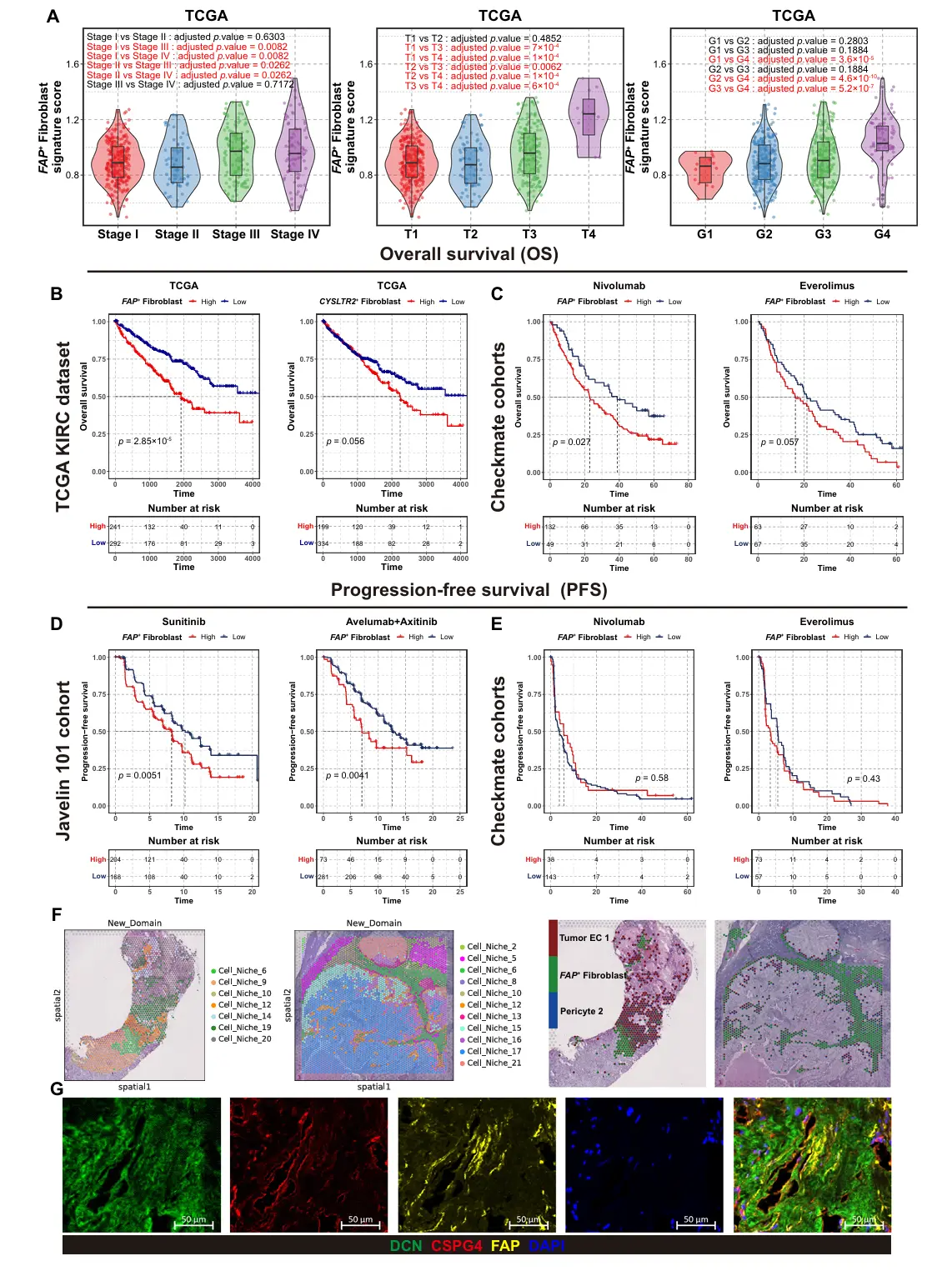
结果6、FAP+ 成纤维细胞富集预示RCC不良预后及抗VEGF治疗耐药
临床关联: FAP+成纤维细胞的富集与肾癌的更晚期阶段、更高恶性程度以及更差的患者总生存期密切相关。
关键发现(治疗预测): FAP+成纤维细胞是预测抗VEGF靶向治疗耐药的潜在生物标志物。在接受含抗VEGF药物治疗的患者中,高FAP+成纤维细胞评分预示着更短的无进展生存期,但在不接受此类药物的治疗方案中则无此预测作用。
潜在机制提示: FAP+成纤维细胞在肿瘤内紧密环绕血管分布,这种特殊的空间位置可能介导了其对血管靶向药物的抵抗机制。
角色定位: 它更像是整体侵袭性肿瘤微环境的一个标志和推动者,其预后价值可能被更传统的临床病理因素(如分期、分级)所涵盖,但其在预测特定疗法(尤其是抗VEGF治疗)疗效方面具有独特且重要的价值。
最后,我们来看看方法
单细胞部分



空间转录组部分



生活很好,有你更好
 https://mp.weixin.qq.com/s/8E1vYJMNhe5m0DXieBHfzA, 做生信8年了,我会针对单细胞空间常用的基础内容进行培训,让大家掌握基础的Linux、R、和python,让大家分析单细胞空间外显子,基础的内容不会成为卡点,看到想分析的内容,可以通过思想把代码构思并且实现出来。
https://mp.weixin.qq.com/s/8E1vYJMNhe5m0DXieBHfzA, 做生信8年了,我会针对单细胞空间常用的基础内容进行培训,让大家掌握基础的Linux、R、和python,让大家分析单细胞空间外显子,基础的内容不会成为卡点,看到想分析的内容,可以通过思想把代码构思并且实现出来。












