AbMole小课堂 | Nivolumab(BMS-936558):PD-1人源化单抗的作用机制与抗肿瘤应用
Nivolumab作为一种免疫检查点抑制剂,自问世以来在科研领域引发了广泛而深入的研究。Nivolumab通过阻断免疫检查点PD-1(即程序性死亡受体1,CD279)信号通路,起到了重塑机体免疫平衡、激活免疫细胞抗肿瘤活性的作用。
一、Nivolumab(BMS-936558)的作用原理
免疫检查点是免疫系统中用于调节T细胞活性的分子机制,其主要功能是防止免疫反应过度,维持免疫耐受。免疫检查点分子包括CTLA-4、PD-1、PD-L1等。在众多免疫细胞亚群中,细胞毒性 T 淋巴细胞(CTL)是直接杀伤肿瘤的关键效应细胞。肿瘤细胞表面往往会高表达PD -L1,并通过PD-L1与CTL表面的PD-1结合,抑制CTL的杀伤功能。Nivolumab(纳武单抗,BMS-936558,AbMole,M6100)是一种靶向PD-1的免疫球蛋白G4单克隆抗体。Nivolumab 能够结合PD-1,阻断PD-1/PD-L1信号轴,解除免疫抑制,使CTL重新获得对肿瘤细胞的识别和杀伤能力。此外,Nivolumab还能够影响辅助性 T 细胞(Th)亚群的平衡,Nivolumab可促进Th1型细胞因子的分泌,增强细胞免疫应答,同时抑制Th2型免疫反应,减少免疫抑制环境的形成。这种机制有助于打破肿瘤微环境中的免疫抑制状态,使免疫系统更有效地攻击肿瘤细胞[1]。
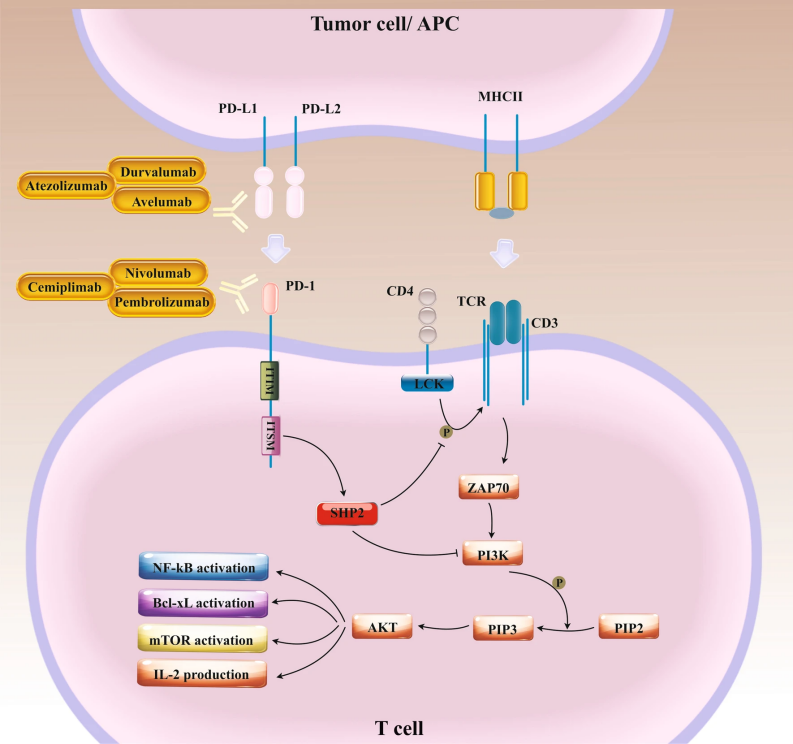
图 1.免疫检查点及其抑制剂[2]
二、Nivolumab(BMS-936558)的研究应用
Nivolumab(纳武利尤单抗,BMS-936558,AbMole,M6100)可用于多种肿瘤的抑制,例如黑色素瘤、非小细胞肺癌(NSCLC)、头颈部鳞状细胞癌(HNSCC)、食管癌、肝细胞癌[3]。Nivolumab也是联合抑制策略研究中常用的生物活性分子,例如Nivolumab 与伊匹木单抗(Ipilimumab,一种 CTLA-4 抑制剂)的联合应用在黑色素瘤治疗中取得了显著成果[4]。在肺癌研究中,Nivolumab 与多种抑制剂之间都表现出了协同增效的作用,例如Nivolumab联合Cisplatin(顺铂)的抑制方案,较单一处理组显著延长了非小细胞肺癌小鼠的生存曲线[5, 6]。此外,Nivolumab与其他靶向抑制剂如小分子酪氨酸激酶抑制剂的联合研究也在进行中。通过同时阻断肿瘤细胞的多个关键信号通路以及激活免疫系统,有望进一步提高抑制效果[7, 8]。
三、范例详解
Mol Cell Probes. 2023 Dec;72:101925.
西南医科大学,清迈大学的研究团队在上述文章中发现了黑色素瘤对PD-1抑制剂耐药的新型生物标志物。研究表明,CD3ζ在PD-L1阴性(IHC PD-L1(−))的黑色素瘤细胞中显著下调,低表达CD3ζ与较差的预后、更低的肿瘤免疫浸润水平以及对PD-1抑制剂(如Nivolumab)的耐药高度相关。通过体内外实验,实验人员进一步证实:补充CD3ζ可增强Nivolumab对耐药黑色素瘤的杀伤效果。由AbMole提供的Nivolumab(纳武单抗,BMS-936558,AbMole,M6100)在上述实验中起到了重要的作用,实验人员通过逐步增加Nivolumab浓度的方式处理B16–F10细胞,建立Nivolumab耐药细胞系(B16–F10R)。
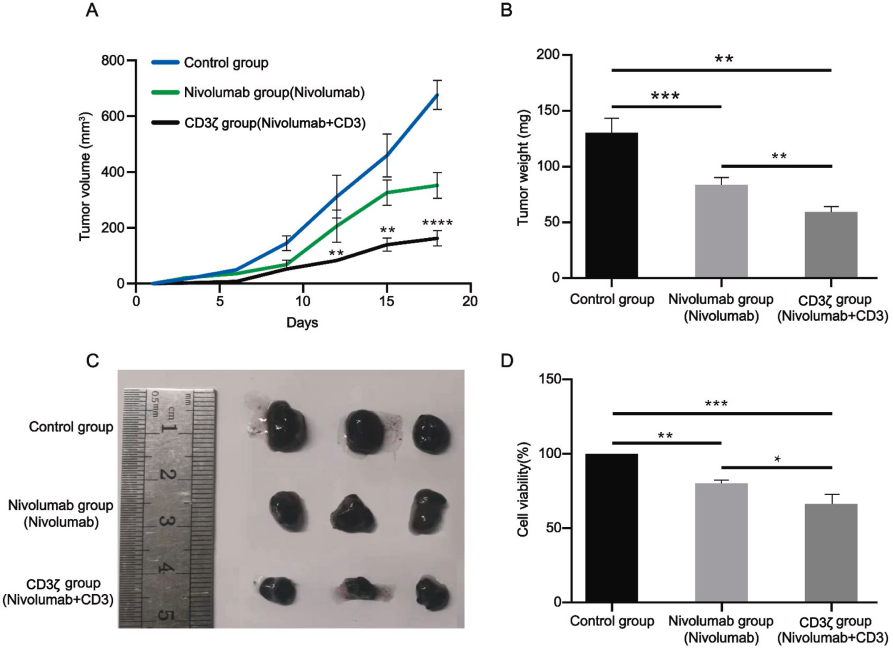
图 2. Increase CD3ζ can potentiates anti-PD-1 treatment efficacy[9].
AbMole是ChemBridge中国区官方指定合作伙伴。

参考文献及鸣谢
[1] G. Losurdo, D. Angelillo, N. Favia, et al., Checkpoint Inhibitor-Induced Colitis: An Update, Biomedicines 11(5) (2023).
[2] A. Naimi, R. N. Mohammed, A. Raji, et al., Tumor immunotherapies by immune checkpoint inhibitors (ICIs); the pros and cons, Cell communication and signaling : CCS 20(1) (2022) 44.
[3] S. Yust-Katz, E. Dudnik, E. Perlov, et al., P13.10 Intracranial response to nivolumab in NSCLC patients with untreated or progressing CNS metastases, (suppl_4) (2016) iv71-iv71.
[4] 张珉, 钟武等, 临床药物治疗杂志, 黑色素瘤治疗新组合——Nivolumab和Ipilimumab, (2017).
[5] The Luc Ma, Stephanie Daignault, Jessica Waninger, et al., The impact of BRAF mutation status on clinical outcomes with single-agent PD-1 inhibitor versus combination ipilimumab/nivolumab, 38(15_suppl) (2020) 10024-10024.
[6] Wei Chi, Lianyong Zhang, Xue Wang, et al., Effects of Nivolumab and Ipilimumab on the suppression of cisplatin resistant small cell lung cancer cells, (4) (2022) 40.
[7] David Aggen, Meredith Mckean, Nehal Lakhani, et al., 661Initial results from a phase 1a/b study of IK-175, an oral AHR inhibitor, as a single agent and in combination with nivolumab in patients with advanced solid tumors and urothelial carcinoma, 10(Sup2) (2022) 1.
[8] Yann Alexre Vano, Réza Elaidi, Mostefa Bennamoun, et al., Nivolumab, nivolumab-ipilimumab, and VEGFR-tyrosine kinase inhibitors as first-line treatment for metastatic clear-cell renal cell carcinoma (BIONIKK): a biomarker-driven, open-label, non-comparative, randomised, phase 2 trial, (5) (2022) 23.
[9] Z. Zhang, D. Zhang, F. Wang, et al., CD3ζ as a novel predictive biomarker of PD-1 inhibitor resistance in melanoma, Molecular and cellular probes 72 (2023) 101925.
