中科院1区顶刊|IF14+:多组学MR联合单细胞时空分析,锁定心血管代谢疾病的免疫治疗新靶点

中科院1区顶刊|IF14+:多组学MR联合单细胞时空分析,锁定心血管代谢疾病的免疫治疗新靶点
当下,免疫与代谢性疾病的关联研究已成为生命科学领域的前沿热点。随着研究的深入,我们愈发清晰地认识到免疫系统与代谢系统之间存在着极为复杂且紧密的交互网络,这种交互失衡在诸如2型糖尿病、冠状动脉疾病等慢性疾病的发生发展进程中扮演着关键角色。与此同时,孟德尔随机化(MR)这一强大的因果推断工具,在结合多组学数据尤其是单细胞动态数据方面,展现出了巨大的潜力,为突破传统研究局限,精准解析疾病分子机制提供了新的路径。而精准确定药物靶点,作为连接基础研究与临床治疗的关键桥梁,始终是新药研发领域的核心挑战与焦点。在此背景下,一篇发表于Nature Communications的研究论文,凭借其创新的研究策略和卓越的研究成果,为我们带来了全新的视角与深刻的启示。
https://doi.org/10.1038/s41467-024-53621-7

正式介绍
基本信息
-
论文标题:CD4+ T细胞激活过程的全转录组MR研究揭示心血管代谢疾病的免疫相关药物靶点
-
发表期刊:Nature Communications,中科院综合性期刊1区Top,IF=14.7007
-
发表日期:2024年10月28日在线发表
研究背景
免疫系统与代谢疾病的交叉证据:免疫系统在2型糖尿病(T2D)和冠状动脉疾病(CAD)等代谢疾病中的作用逐渐被揭示,如IL-6受体抑制剂在心血管疾病中的临床应用,但CD4+ T细胞激活过程中的基因表达动态与疾病的因果关系仍不明确。传统研究的局限性:多数研究基于bulk组织eQTL,无法捕捉细胞类型特异性和激活时间点的动态效应,而单细胞技术的发展为解析CD4+ T细胞激活的时空基因表达调控提供了可能。MR方法的优势:孟德尔随机化可利用遗传变异作为工具变量,推断基因表达与疾病的因果关系,避免传统关联分析的反向因果和混杂偏倚,是药物靶点优先级排序的强大工具。
研究思路
数据整合:整合CD4+ T细胞激活5个时间点(0 h、LA、16 h、40 h、5 d)的单细胞eQTL数据(119例欧洲个体),构建11,021个基因表达谱与T2D/CAD的GWAS summary数据(DIAGRAM和Aragam等队列)的关联分析队列。因果推断与验证:采用Wald比率、加权中位数等8种MR方法,结合LD clumping、F统计量过滤和Steiger方向检验,筛选因果基因;通过共定位分析和LD check验证因果信号的可靠性;结合单细胞差异表达分析、细胞类型特异性和激活时间点动态效应解析,深化机制理解。药物靶点优先级排序:将MR鉴定的因果基因与相关数据库交叉比对,筛选处于临床研究阶段的药物靶点,并通过通路分析验证其免疫调控机制。
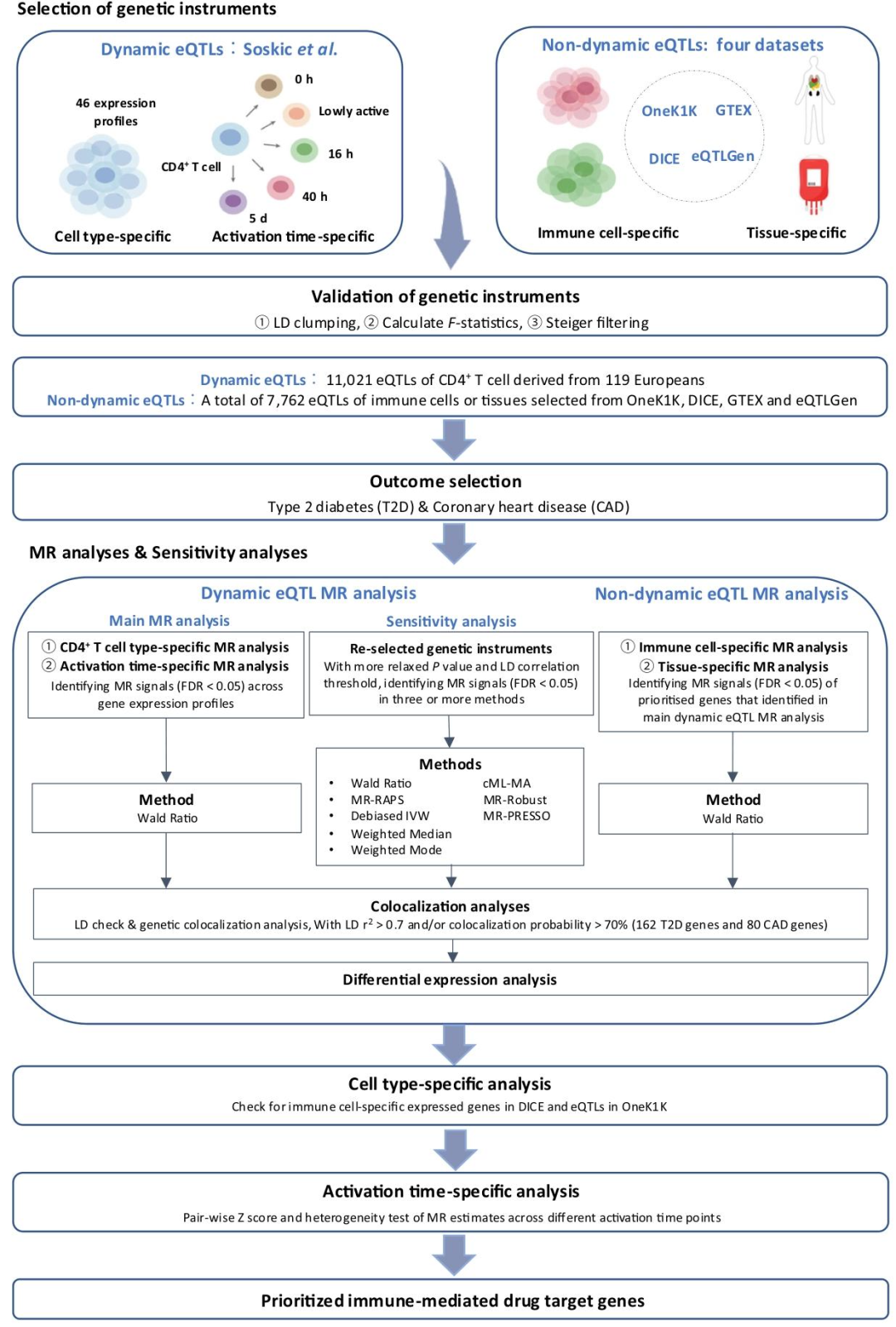
图1 | 动态与非动态eQTL MR分析的研究设计
研究亮点
动态单细胞eQTL与MR的整合:首次在CD4+ T细胞激活的时空维度上开展全转录组MR分析,发现基因表达的时间特异性因果效应(如HLA-C在CD4+ T细胞激活16 h时对CAD的风险峰值)。细胞类型特异性证据链:通过单细胞表达数据和eQTL跨数据集验证,证实12%的T2D基因和16%的CAD基因具有CD4+ T细胞特异性,突破传统bulk组织研究的局限性。临床转化导向的靶点发现:直接关联25个因果基因与临床在研药物(如LIPA、GCK),其中4个基因(KHK、GCK、ERN1、LIPA)的药物-疾病对已在临床试验中验证,为药物再利用提供精准线索。
数据来源和生物信息方法
1、数据来源
暴露数据:CD4+ T细胞激活5个时间点的单细胞eQTL数据(Soskic et al., 2022),涵盖17种细胞类型、46个表达谱、13,379个基因的482,971个eQTL;疾病数据:T2D(DIAGRAM consortium,80,154例vs. 853,816对照)和CAD(Aragam et al., 181,522例vs. 984,168对照)的GWAS summary数据(欧洲人群);验证数据:4个非动态eQTL数据集(OneK1K、DICE、GTEx v8、eQTLGen),以及7个单细胞差异表达数据集(T2D与对照的免疫细胞测序数据)。
2、生物信息方法
MR分析:工具变量筛选:LD clumping(r²<0.001)、F统计量>10、Steiger方向检验;核心方法:Wald比率(单工具变量)、加权中位数、加权模式、MR-PRESSO等8种敏感性分析方法;共定位分析:Coloc包(后验概率>70%)和LD check(r²>0.7)。动态与细胞类型特异性分析:时间点异质性检验:Cochrane Q检验、成对Z检验;细胞类型特异性:熵方法(entropy method)、单细胞差异表达分析(Seurat包)、跨数据集eQTL验证(OneK1K、DICE)。药物靶点分析:数据库整合:DrugBank、OpenTargets、ClinicalTrials.gov;通路富集:Metascape、STRING蛋白互作网络分析。
主要结果
1、动态eQTL-MR鉴定T2D和CAD的因果基因
在15,982个基因-疾病对中,766个基因-T2D对和211个基因-CAD对通过FDR<0.05筛选,其中652个T2D对和197个CAD对经共定位验证(图2);鉴定出162个T2D因果基因和80个CAD因果基因,其中121个T2D基因(75%)和45个CAD基因(56%)已在OpenTargets数据库中报道(图2)。小结:动态eQTL-MR成功识别大量免疫相关因果基因,且与已知疾病关联基因高度重叠,验证了方法的可靠性。
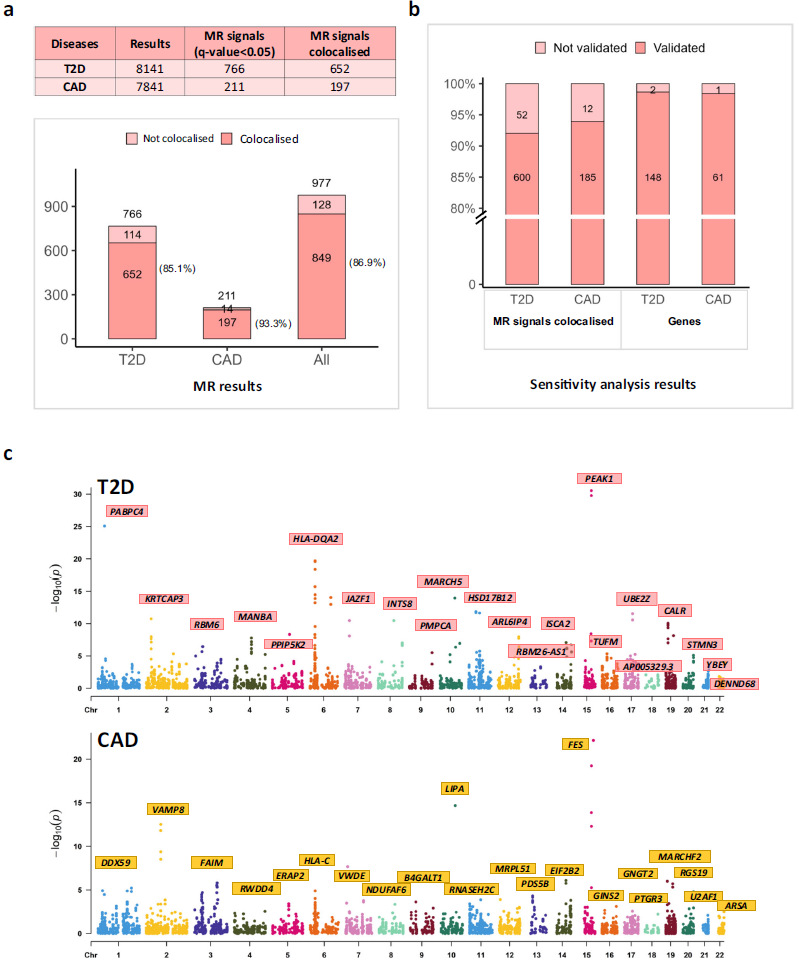
图2 | CD4+ T细胞动态eQTL对T2D和CAD因果效应的MR结果及顶级靶点基因
2、细胞类型特异性分析
因果基因主要富集于记忆CD4+ T细胞和效应记忆T细胞,其MR信号数量与Soskic等报道的eGene数量呈强相关(图5);14%的T2D基因和10%的CAD基因在T细胞中特异性表达,且与其他免疫细胞的表达相关性低(图5)。小结:CD4+ T细胞激活过程中,记忆和效应T细胞亚群是免疫-代谢疾病关联的关键细胞类型。
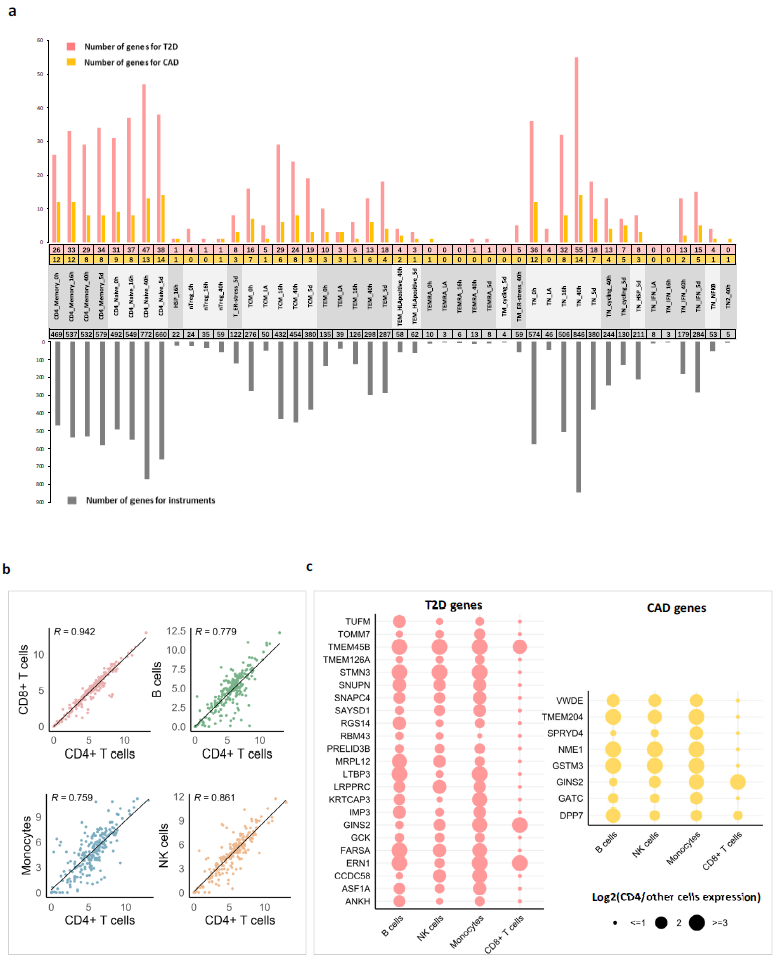
图5 | 细胞类型特异性分析结果
3、激活时间点特异性因果效应
149个基因(67.1%)仅在激活状态下显示MR效应,如MRPL21和GCDH在记忆CD4+ T细胞激活40 h时对T2D的风险效应达到峰值(图6);69个基因-T2D对和34个基因-CAD对存在时间点异质性,且这类基因更可能具有强MR证据(T2D:9.5倍,CAD:7.8倍,图6)。小结:CD4+ T细胞激活的动态过程中,基因表达的时间特异性是驱动疾病风险的重要因素,捕捉时间效应可提升因果推断的可靠性。
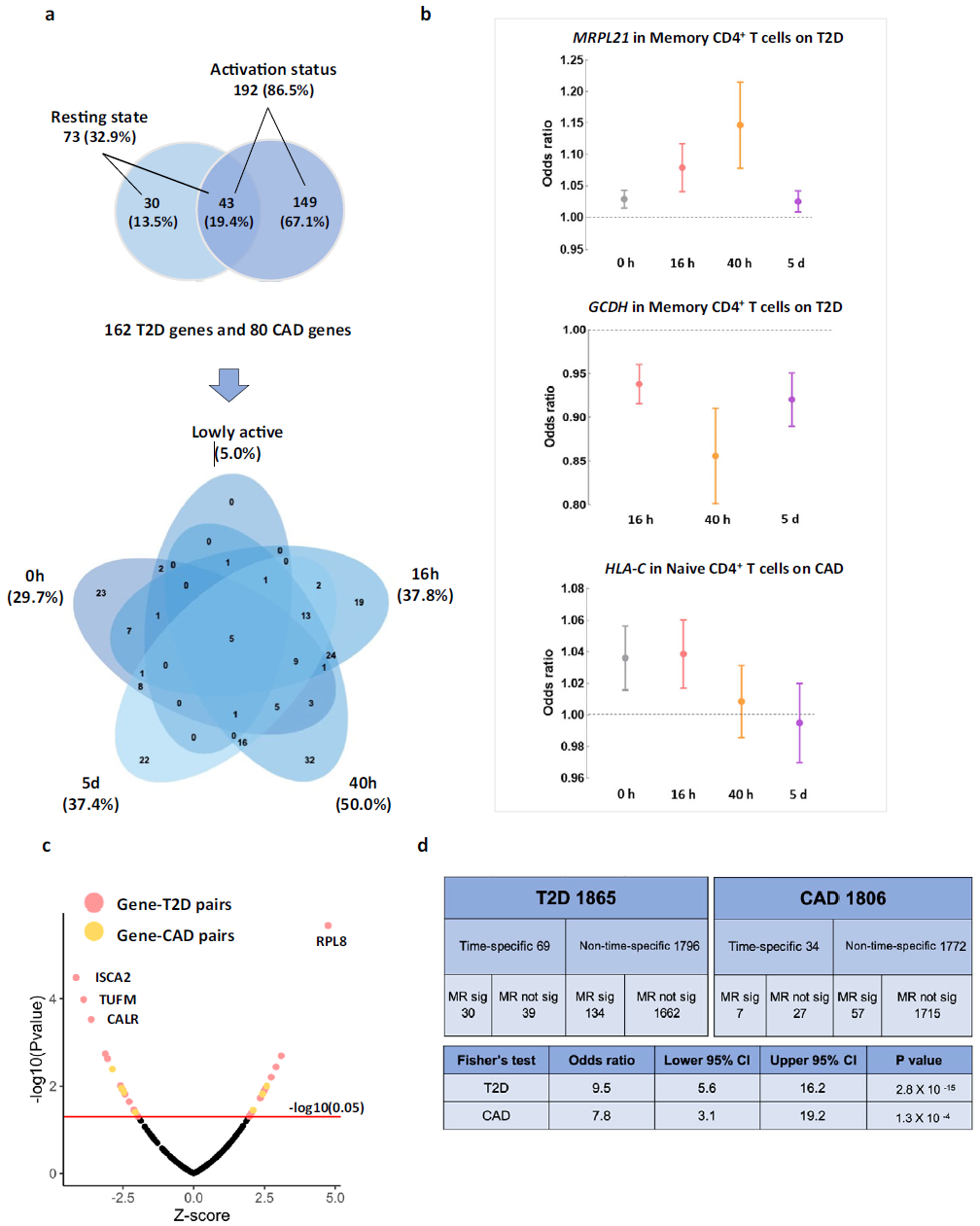
图6 | 不同激活时间点的基因分布、成对Z分数和MR估计值异质性检验
4、免疫相关药物靶点优先级排序
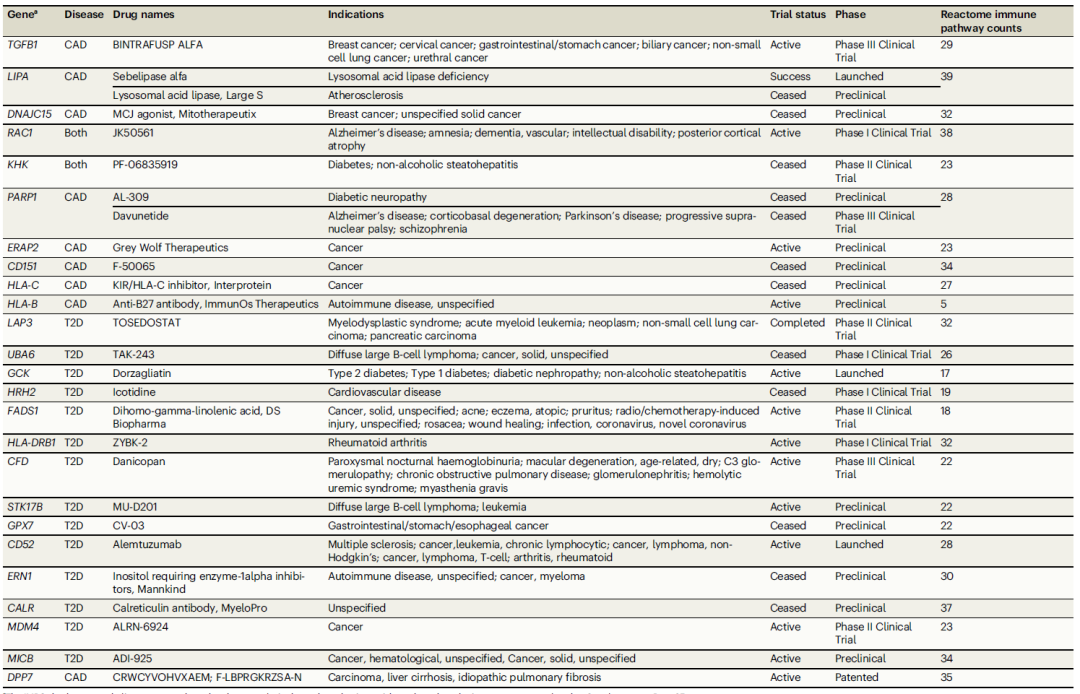
25个因果基因对应临床在研药物,如LIPA(已获批用于溶酶体酸性脂肪酶缺乏症,临床试验用于动脉粥样硬化)、GCK(表1);ERAP2抑制剂在癌症治疗中处于临床前阶段,本研究显示其表达降低与CAD风险下降相关(OR=1.02,95%CI 1.01-1.03,P=7.3×10⁻⁶),提示免疫调节药物再利用潜力。小结:MR因果基因与临床药物的直接关联,为心血管代谢疾病的免疫治疗提供了可转化的靶点清单。
表1 | 具有随机临床试验证据的基因详细信息
研究结论
本研究通过动态单细胞eQTL与全转录组MR的整合分析,系统解析了CD4+ T细胞激活过程中基因表达对T2D和CAD的因果效应,鉴定出162个T2D和80个CAD因果基因,其中10%-16%具有CD4+ T细胞特异性。激活时间点分析揭示基因表达的时间动态是疾病风险的关键驱动因素,而临床转化分析进一步锁定25个免疫相关药物靶点。本项研究结果不仅深化了免疫-代谢交互作用的机制理解,更为心血管代谢疾病的免疫调节治疗提供了精准的靶点方向。
研究的局限性和未来方向
局限性:动态eQTL数据仅覆盖欧洲人群,缺乏其他种族验证;基因表达的因果效应基于遗传预测,需结合蛋白水平和功能实验验证;反向MR分析受限(仅通过Steiger检验排除反向因果)。
未来方向:整合多种族动态eQTL数据,提升结果普适性;结合单细胞蛋白组和功能实验(如CRISPR筛选),验证因果基因的功能机制;拓展至其他免疫细胞类型,构建更全面的免疫-代谢疾病网络。
感谢您的阅读,欢迎关注“生信学术纵览”。谢谢您的分享、点赞+在看!
