基于自校准分数的扩散模型在并行磁共振成像中联合进行线圈灵敏度校正和运动校正|文献速递-深度学习医疗AI最新文献
Title
题目
Joint coil sensitivity and motion correction in parallel MRI with aself-calibrating score-based diffusion model
基于自校准分数的扩散模型在并行磁共振成像中联合进行线圈灵敏度校正和运动校正
01
文献速递介绍
磁共振成像(MRI)在临床诊断和基础研究领域均是处于领先地位的成像方式。然而,MRI的一个主要弊端在于其数据采集时间较长。为解决这一问题,已开发出多种加速技术,使得能够从部分采样的k空间数据中重建出高质量的MRI图像。并行成像利用多个接收线圈之间的信息冗余来实现加速,并且在常规临床扫描中得到了广泛应用(格里斯沃尔德等人,2002年;普吕斯曼等人,1999年)。此外,压缩感知理论提供了一种更为高效的加速MRI的方法,它要求对k空间进行随机欠采样,并在变换域中应用稀疏约束,以减轻重建过程中出现的非相干伪影(勒斯蒂格等人,2007年;奥塔索等人,2010年)。近年来,深度学习已成为加速MRI的一种强大工具。这些以监督或自监督方式训练神经网络的方法,在该领域取得了显著成就(阿加瓦尔等人,2018年;亚曼等人,2020年;吴等人,2024年;赵等人,2024年)。尽管付出了这些努力,但MRI在数据采集过程中仍然容易受到患者运动的影响,从而导致产生各种类型的伪影,降低了重建图像的质量(戈登施韦格等人,2016年)。图像质量的下降可能会产生无法用于诊断的信息,这可能需要重新扫描,进而导致治疗延误和医疗成本增加。此外,未检测到的运动伪影存在产生假阳性或假阴性结果的风险(安德烈等人,2015年)。 此前,运动校正这一挑战已通过两种主要方法得到广泛处理:前瞻性和回顾性策略。前瞻性运动校正涉及调整采集过程,以补偿所测量到的刚体运动。这种方法通常需要使用导航器或额外的运动探测器来修改脉冲序列,这会增加扫描过程的复杂性,并可能延长扫描时间。另一方面,回顾性方法在数据采集后通过算法来处理运动校正问题,无需对外部硬件进行修改。回顾性技术可分为两种主要方法。第一种方法(乌斯曼等人,2020年;阿尔马尼奥等人,2020年;约翰逊和德朗戈娃,2019年)将运动校正视为一个图像后处理问题(即去模糊)。然而,这些方法忽略了MRI采集的物理正向模型,导致在参数估计和图像重建方面的性能欠佳。第二种工作思路是将先验运动信息纳入物理模型中,该模型考虑了患者运动对k空间数据的影响。基于模型的方法通过最大化数据一致性,以交替或联合的方式优化图像和运动参数(哈斯克尔等人,2018年;科尔德罗 - 格兰德等人,2018年;巴彻勒等人,2005年)。尽管这些方法具有潜力,但重建问题的非凸性和高度不适定性带来了重大挑战,并且这些方法在临床应用中往往难以提供稳定的性能(霍斯巴赫等人,2023年)。 基于分数的扩散模型的出现彻底改变了解决逆问题的方法,提供了强大的深度生成先验。这些模型在各种任务中(例如图像修复、图像超分辨率,钟等人,2022c、a以及医学成像,宋等人,2021年;贾拉尔等人,2021年;钟和叶,2022年;莱瓦茨等人,2023年;吴等人,2024年;拉武拉等人,2023年)展现出了巨大的潜力。为了加速MRI,几种基于扩散模型的方法已经取得了显著进展(钟和叶,2022年;贾拉尔等人,2021年;彭等人,2023年;于等人,2023年;崔等人,2023年;曹等人,2024年;崔等人,2022年;关等人,2024年)。然而,使用基于分数的扩散模型来解决欠采样MRI采集中的运动校正挑战尚未得到充分探索。最近,莱瓦茨等人(2023年)提出了一种方法,该方法使用基于分数的扩散模型联合重建欠采样的MRI数据并估计运动参数,在运动校正方面实现了当前最优(SOTA)性能。 然而,现有的基于模型和基于分数的方法都忽略了运动对估计的线圈灵敏度图(CSMs)的影响,而线圈灵敏度图对于多线圈欠采样MRI重建至关重要(王等人,2024年;孙等人,2024年)。通常,这些方法假设线圈灵敏度图是预先确定的,没有考虑运动因素,或者假设运动不会影响用于校准的k空间的全采样中心部分。然而,尽管在脑部MRI扫描期间射频(RF)线圈通常是固定的,但由于运动,头部相对于射频线圈的相对位置会发生变化,从而导致实际的线圈灵敏度发生变化。一般来说,灵敏度图不仅受到相对于线圈的位置偏移的影响,还受到由运动引起的电磁特性(如介电常数和电导率)变化的影响。这些影响在较高的场强下尤为明显(波夫拉多·罗德里格斯等人,2021年),在这种情况下,它们会显著影响发射射频空间轮廓。因此,在自动校准k空间区域的采集过程中,任何不可避免的运动(例如癫痫患者的运动)都可能引入运动伪影,降低重建图像的质量。 在本文中,我们提出了一种自校准方法,用于加速MRI重建,该方法联合估计运动参数和线圈灵敏度图(JSMoCo)。这种联合优化确保了系统的一致性,并避免了因运动而损坏的预估计灵敏度图所产生的误差,从而得到无明显伪影的高质量MRI图像。联合优化增加了未知量的数量,使得逆问题的不适定性更强。为了解决这个问题,我们引入基于分数的扩散模型作为强大的先验,并利用多线圈MRI的物理采集过程来有效地约束解空间。具体而言,我们使用三个可训练变量(一个旋转角度和两个平移偏移量)对二维运动参数进行参数化,以准确地模拟刚体运动。此外,我们使用一组多项式函数对时变线圈灵敏度图进行参数化,明确地强制其具有连续和光滑的特性。最后,将运动参数、线圈灵敏度图和重建的MRI图像的联合优化建模为一个盲逆问题。受近期进展(村田等人,2023年)的启发,并利用物理知识,我们采用吉布斯采样器(卡塞拉和乔治,1992年)通过从联合后验分布中采样来优化这些参数。 为了评估所提出方法的有效性,我们在fastMRI数据集(诺尔等人,2020年)上进行了模拟实验,并对采集的受运动影响的T2加权脑部扫描进行了体内实验,实验采用了不同的加速因子。此外,我们还评估了所提出方法在平面外运动情况下的性能。定性和定量结果表明,JSMoCo能够在不同的加速因子、运动水平和运动类型下稳健地生成伪影较少的重建结果。这项工作的主要贡献总结如下: 1. 据我们所知,JSMoCo是第一种考虑运动对线圈灵敏度图影响的方法。估计的时变线圈灵敏度准确地反映了头部相对于射频线圈的相对运动。通过采用联合优化策略,JSMoCo有效地减轻了从预估计的灵敏度图到最终重建图像的误差传播,最终得到伪影减少的高质量图像。 2. JSMoCo将多线圈MRI采集过程与刚体运动纳入基于分数的扩散先验中,有效地约束了解空间,并优化了高度不适定的逆问题。 3. 我们的结果表明,JSMoCo在准确估计不同运动模式下的运动参数和时变线圈灵敏度图的同时,能够出色地生成高质量的重建结果。
Abatract
摘要
Magnetic Resonance Imaging (MRI) stands as a powerful modality in clinical diagnosis. However, it faceschallenges such as long acquisition time and vulnerability to motion-induced artifacts. While many existingmotion correction algorithms have shown success, most fail to account for the impact of motion artifacts oncoil sensitivity map (CSM) estimation during fast MRI reconstruction. This oversight can lead to significantperformance degradation, as errors in the estimated CSMs can propagate and compromise motion correction.In this work, we propose JSMoCo, a novel method for jointly estimating motion parameters and timevarying coil sensitivity maps for under-sampled MRI reconstruction. The joint estimation presents a highlyill-posed inverse problem due to the increased number of unknowns. To address this challenge, we leveragescore-based diffusion models as powerful priors and apply MRI physical principles to effectively constrainthe solution space. Specifically, we parameterize rigid motion with trainable variables and model CSMs aspolynomial functions. A Gibbs sampler is employed to ensure system consistency between the sensitivity mapsand the reconstructed images, effectively preventing error propagation from pre-estimated sensitivity mapsto the final reconstructed images. We evaluate JSMoCo through 2D and 3D motion correction experimentson simulated motion-corrupted fastMRI dataset and in-vivo real MRI brain scans. The results demonstratethat JSMoCo successfully reconstructs high-quality MRI images from under-sampled k-space data, achievingrobust motion correction by accurately estimating time-varying coil sensitivities.
磁共振成像(MRI)是临床诊断中一种强大的成像方式。然而,它面临着诸如采集时间长以及易受运动引起的伪影影响等挑战。尽管许多现有的运动校正算法已取得了成功,但大多数算法在快速磁共振成像重建过程中未能考虑运动伪影对线圈灵敏度图(CSM)估计的影响。这种疏忽可能会导致性能大幅下降,因为估计的线圈灵敏度图中的误差可能会传播并影响运动校正的效果。 在这项工作中,我们提出了JSMoCo,这是一种用于联合估计运动参数和时变线圈灵敏度图的新方法,适用于欠采样磁共振成像的重建。由于未知量的增加,联合估计会带来一个高度不适定的逆问题。为应对这一挑战,我们利用基于分数的扩散模型作为强大的先验信息,并应用磁共振成像的物理原理来有效地约束解空间。具体而言,我们使用可训练变量对刚体运动进行参数化,并将线圈灵敏度图建模为多项式函数。采用吉布斯采样器来确保灵敏度图与重建图像之间的系统一致性,有效地防止预估计的灵敏度图中的误差传播到最终的重建图像中。我们通过在模拟的受运动影响的快速磁共振成像数据集以及体内真实的脑部磁共振扫描数据上进行二维和三维运动校正实验,对JSMoCo进行了评估。结果表明,JSMoCo能够从欠采样的k空间数据中成功重建高质量的磁共振图像,通过准确估计时变的线圈灵敏度来实现稳健的运动校正。
Method
方法
While existing retrospective motion correction methods (Haskellet al., 2018, 2019; Usman et al., 2020; Levac et al., 2023) have showngreat performance, they face a fundamental limitation: the need foraccurate coil sensitivity maps for effective motion estimation and imagereconstruction. However, the relative motion during MRI acquisitioninevitably leads to variations in coil sensitivity due to positional shiftsrelative to the RF coil.In this work, we assume the head motion is rigid and model thesensitivity maps as a set of polynomial functions (Ying and Sheng,2007). We then jointly optimize the image and the unknown parameters associated with both motion and sensitivity maps. This approacheffectively mitigates the propagation of errors from the sensitivity mapsto the final reconstructed image. Consequently, our proposed methodcan reconstruct high-quality MRI images even in the presence of motioncorruption, particularly in scenarios requiring accurate coil sensitivityestimation, e.g., k-space autocalibration regions.
尽管现有的回顾性运动校正方法(哈斯克尔等人,2018年、2019年;乌斯曼等人,2020年;莱瓦茨等人,2023年)已展现出优异的性能,但它们面临一个根本性的局限:在进行有效的运动估计和图像重建时,需要精确的线圈灵敏度图。然而,在磁共振成像(MRI)数据采集过程中的相对运动,不可避免地会因相对于射频线圈的位置偏移而导致线圈灵敏度发生变化。 在这项工作中,我们假定头部运动为刚体运动,并将灵敏度图建模为一组多项式函数( Ying 和 Sheng,2007年)。然后,我们联合优化图像以及与运动和灵敏度图相关的未知参数。这种方法有效地减轻了从灵敏度图到最终重建图像的误差传播。因此,我们提出的方法即使在存在运动干扰的情况下,也能够重建出高质量的磁共振图像,尤其是在需要精确估计线圈灵敏度的场景中,例如k空间自动校准区域。
Conclusion
结论
We propose JSMoCo, a novel unsupervised MRI reconstructionmethod that takes into account rigid motion during image acquisition.Different from the existing motion correction methods, our model considers the effect of motion on the coil sensitivity maps. By incorporatingthe multi-coil MRI acquisition process with parameterized rigid motionand coil sensitivities into the score-based diffusion priors, we effectivelyleverage the Gibbs sampler to jointly optimize MRI images, motionparameters, and coil sensitivity maps. Experimental results conductedon the fastMRI dataset and real acquired MRI data demonstrate thesuperiority of our approach in reconstructing high-quality MRI imagesfrom motion-corrupted and under-sampled k-space measurements.
我们提出了JSMoCo,这是一种新颖的无监督磁共振成像(MRI)重建方法,该方法考虑了图像采集过程中的刚体运动。与现有的运动校正方法不同,我们的模型考虑了运动对线圈灵敏度图的影响。通过将多线圈MRI采集过程与参数化的刚体运动以及线圈灵敏度纳入基于分数的扩散先验中,我们有效地利用吉布斯采样器来联合优化MRI图像、运动参数和线圈灵敏度图。在fastMRI数据集和实际采集的MRI数据上进行的实验结果表明,我们的方法在从受运动干扰且欠采样的k空间测量数据中重建高质量的MRI图像方面具有优越性。
Results
结果
5.1. Simulated motion correction experimental results5.1.1. Comparisons of the reconstruction MR images*Fig. 2 displays a representative slice reconstructed by differentmethods with fixed motion offsets and different acceleration factors.At 𝑅 = 2, reconstruction results of ZF and L1-Wavelet suffer fromnoticeable motion and aliasing artifacts, primarily stemming from therigid motion corruption. In contrast, motion correction with ScoreMoCo (corrupted CSM) demonstrates improved reconstruction qualitybut still struggles with certain suboptimal reconstructions due to theeffect of motion on the estimated coil sensitivities. Our method, whichjointly optimizes the sensitivity maps during the reconstruction process,yields faithful MR images. It effectively eliminates motion and aliasingartifacts, demonstrating comparable performance to Score-MoCo (withIdeal CSM), as illustrated in the zoomed-in images in Fig. 2. Similarresults are observed when the acceleration factor is raised to 4 and4.8. Particularly, Score-MoCo with corrupted CSM introduces visibleartifacts with a higher acceleration factor. In contrast, our methodmaintains competitive artifact-reduction results comparable to GT andScore-MoCo (Ideal CSM). These results demonstrate the robustness ofour method in handling higher acceleration factors.Table 2 reports the quantitative evaluation metrics analyzed on thesimulation brain dataset with different acceleration factors and motionsettings. The ZF and L1-Wavelet are vulnerable to corrupted sensitivity maps and motion offsets, producing poor reconstruction results.Our proposed model outperforms Score-MoCo (corrupted CSM) andachieves competitive reconstruction errors when compared to ScoreMoCo (Ideal CSM) across all motion settings. For example, our methodachieves a PSNR of 33.13 dB, which is more than 3 dB higher thanthe PSNR achieved by Score-MoCo (corrupted CSM) at 𝑅 = 4.8 withthe motion offset (±2◦&±3) pixels. Notably, at 𝑅 = 4.8, JSMoCodemonstrates a comparable reconstruction performance as the ScoreMoCo (Ideal CSM). This is primarily attributed to our joint optimizationstrategy, which yields a consistent and coherent solution, thus ensuringsuperior system consistency.As shown in Fig. 3, we compare the intensity profiles of the operculum to evaluate the reconstructed local image contrast between tissues.The reconstruction results obtained with the proposed JSMoCo andScore-MoCo (Ideal CSM) exhibit sharp signal changes in the intensityprofiles, consistent with the pattern observed on the GT image. However, in the case of Score-MoCo (corrupted CSM), particularly at 𝑅 =4.8, there is a noticeable shift in the intensity profile when comparedto the GT image, indicating the presence of artifacts.
5.1. 模拟运动校正实验结果 5.1.1. 重建磁共振图像的比较 图2展示了在固定运动偏移和不同加速因子下,由不同方法重建的代表性切片。在加速因子 𝑅 = 2 时,零填充(ZF)和基于L1小波(L1-Wavelet)的重建结果存在明显的运动伪影和混叠伪影,这主要源于刚体运动干扰。相比之下,使用ScoreMoCo(带有受损的线圈灵敏度图(CSM))进行的运动校正显示出重建质量有所提高,但由于运动对估计的线圈灵敏度的影响,仍存在一些不太理想的重建情况。我们的方法在重建过程中联合优化灵敏度图,生成了逼真的磁共振图像。如图2的放大图像所示,它有效地消除了运动伪影和混叠伪影,其性能可与Score-MoCo(带有理想的线圈灵敏度图)相媲美。当加速因子提高到4和4.8时,也观察到了类似的结果。特别是,使用受损线圈灵敏度图的Score-MoCo在加速因子较高时会引入明显的伪影。相比之下,我们的方法保持了与真实值(GT)和Score-MoCo(理想的线圈灵敏度图)相当的减少伪影的效果。这些结果证明了我们的方法在处理较高加速因子时的稳健性。 表2报告了在具有不同加速因子和运动设置的模拟脑部数据集上分析得到的定量评估指标。零填充(ZF)和基于L1小波(L1-Wavelet)的方法易受受损的灵敏度图和运动偏移的影响,从而产生较差的重建结果。我们提出的模型优于Score-MoCo(受损的线圈灵敏度图),并且在所有运动设置下,与Score-MoCo(理想的线圈灵敏度图)相比,实现了具有竞争力的重建误差。例如,在加速因子 𝑅 = 4.8且运动偏移为(±2°&±3)像素的情况下,我们的方法实现了33.13 dB的峰值信噪比(PSNR),比Score-MoCo(受损的线圈灵敏度图)所达到的峰值信噪比高出3 dB以上。值得注意的是,在加速因子 𝑅 = 4.8时,JSMoCo展示出与Score-MoCo(理想的线圈灵敏度图)相当的重建性能。这主要归功于我们的联合优化策略,该策略产生了一致且连贯的解决方案,从而确保了卓越的系统一致性。 如图3所示,我们比较了岛盖区域的强度剖面,以评估重建的组织间局部图像对比度。使用我们提出的JSMoCo和Score-MoCo(理想的线圈灵敏度图)得到的重建结果在强度剖面上显示出明显的信号变化,这与在真实值(GT)图像上观察到的模式一致。然而,对于Score-MoCo(受损的线圈灵敏度图),特别是在加速因子 𝑅 = 4.8时,与真实值(GT)图像相比,强度剖面存在明显的偏移,这表明存在伪影。
Figure
图
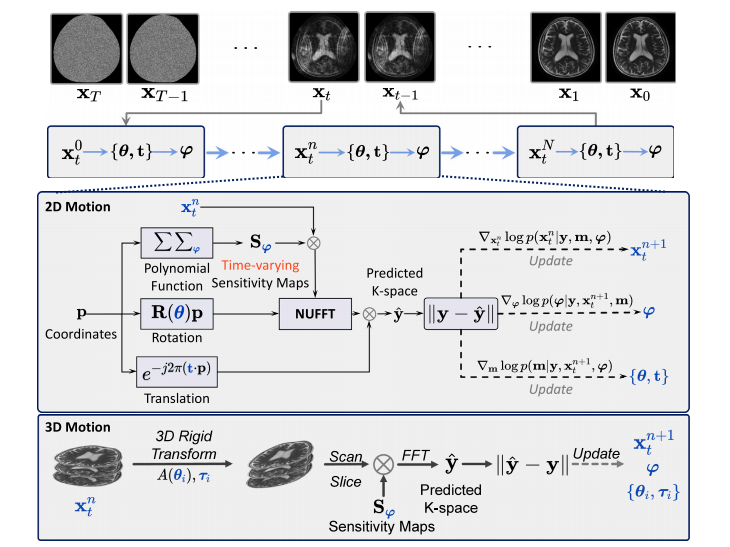
Fig. 1. Overview of the proposed JSMoCo. During the reversing diffusion process (i.e., 𝑡 = 𝑇 → 0), we iteratively sample 𝐱𝑡 , 𝐦 and 𝝋 for a total of 𝑁 times at each timestep 𝑡.The middle box represents the framework for processing 2D motion, while the bottom box represents the framework for processing 3D motion.
图1:所提出的JSMoCo概述。在反向扩散过程中(即,t = T → 0),我们在每个时间步t 迭代采样 𝐱𝑡 、𝐦 和 𝝋,总共采样 N 次。 中间的框表示处理二维运动的框架,而底部的框表示处理三维运动的框架。
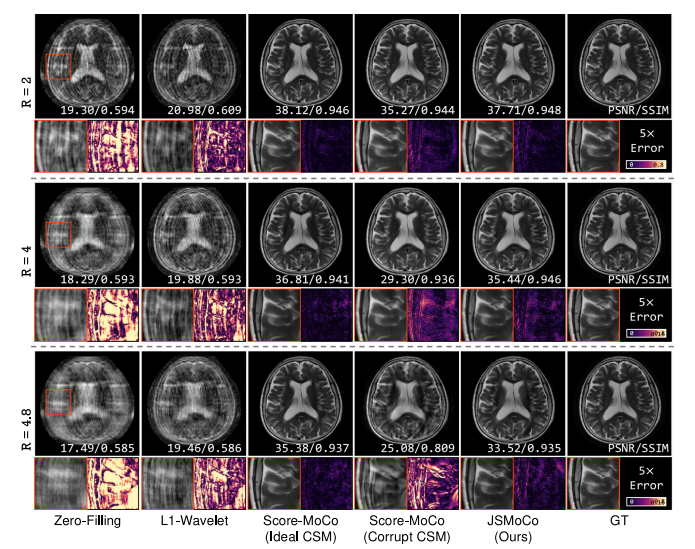
Fig. 2. Qualitative results of the compared methods on the reconstructed images with three accelerated factors (𝑅 = 2, 4, 4.8) that are corrupted by translation of ±3 pixels androtation of ±3◦ . Quantitative evaluation metrics (PSNR and SSIM) are provided above each image. The 5× error maps are displayed for better visualization
图2:在由平移 ±3 像素和旋转 ±3 度所造成干扰的图像上,各对比方法在重建图像方面的定性结果。每个图像上方给出了定量评估指标(峰值信噪比(PSNR)和结构相似性指数(SSIM))。还展示了放大 5 倍的误差图,以便更好地进行可视化。
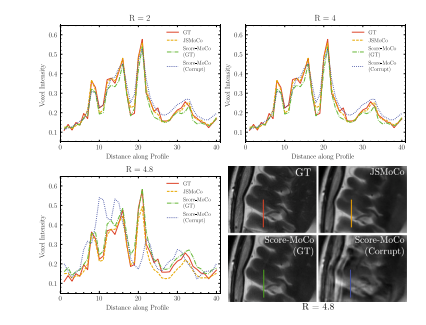
Fig. 3. Comparison of intensity profiles on the reconstructed images obtained usingdifferent methods with simulated data corrupted by translation of ±3 pixels and rotationof ±3◦ .
图3:使用不同方法对受 ±3 像素平移和 ±3 度旋转干扰的模拟数据进行重建,对重建图像的强度轮廓进行比较。
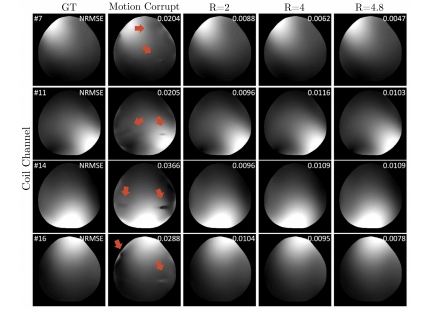
Fig. 4. Qualitative results of estimated CSMs by the proposed method and the ESPIRiTalgorithm using motion-corrupted k-space signal. The red arrows point to the artifactsin the CSMs estimated by ESPIRiT. The coil sensitivity maps from four representativechannels are presented.
图4:所提出的方法和ESPIRiT算法对受运动干扰的k空间信号估计的线圈灵敏度图(CSMs)的定性结果。红色箭头指向由ESPIRiT估计的线圈灵敏度图中的伪影。图中展示了四个具有代表性通道的线圈灵敏度图。
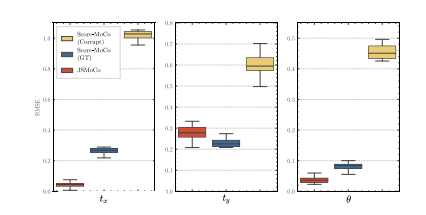
Fig. 5. Comparison of the estimated motion parameters using different methods at𝑅 = 4 corrupted by translation of ±4 pixels and rotation of ±2◦ .
图5:在加速因子R = 4 ,受 ±4 像素平移和 ±2 度旋转干扰的情况下,不同方法对运动参数估计结果的比较。
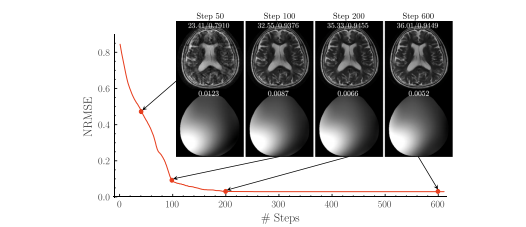
Fig. 6. The convergence of the proposed framework at 𝑅 = 4, corrupted by translation of ±3 pixels and rotation of ±3◦ . The red line represents the NRMSE between estimatedmotion parameters and the ground truth at each step. The top row displays the reconstruction results with PSNR and SSIM values, while the bottom row shows the estimatedCSMs with their respective NRMSE values.
图6:所提出的框架在加速因子R = 4 ,受 ±3 像素平移和 ±3 度旋转干扰情况下的收敛情况。红线表示每一步中估计的运动参数与真实值之间的归一化均方根误差(NRMSE)。顶行展示了带有峰值信噪比(PSNR)和结构相似性指数(SSIM)值的重建结果,而底行展示了估计的线圈灵敏度图及其各自的归一化均方根误差(NRMSE)值。
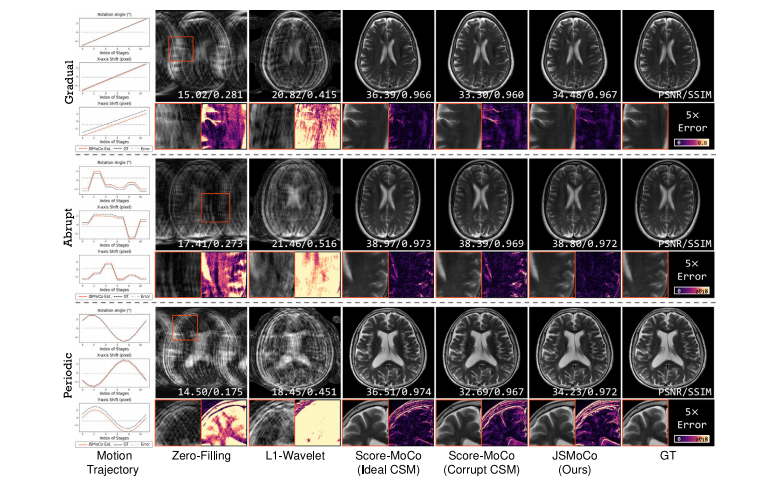
Fig. 7. Qualitative results of JSMoCo applied to simulated motion trajectories (gradual, abrupt and periodic motion) on the fastMRI T2 brain dataset (Knoll et al., 2020), with anacceleration factor of 𝑅 = 4, a motion range of ±3 pixels for translation and ±3 ◦ for rotation
图7:在fastMRI T2脑部数据集(诺尔等人,2020年)上,JSMoCo应用于模拟的运动轨迹(渐变、突变和周期性运动)的定性结果,加速因子R = 4,平移的运动范围为±3像素,旋转的运动范围为±3度。
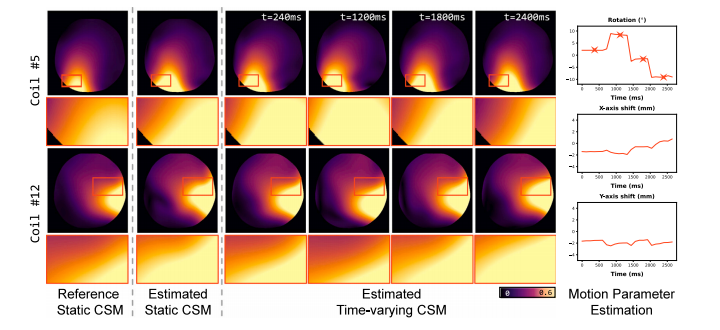
Fig. 8. Qualitative comparisons of the estimated static and time-varying coil sensitivity maps (CSMs) by JSMoCo. The CSMs are visualized using color maps, with zoomed-inregions to better highlight the differences. The temporal changes in the CSMs align well with the estimated motion trajectory, with star markers indicating the specific time pointsassociated with the displayed CSMs.
图8:由JSMoCo估计的静态和时变线圈灵敏度图(CSMs)的定性比较。这些线圈灵敏度图通过彩色图谱进行可视化,并对特定区域进行了放大,以便更好地突出差异。线圈灵敏度图的时间变化与估计的运动轨迹吻合良好,星形标记表示与所显示的线圈灵敏度图相关的特定时间点。
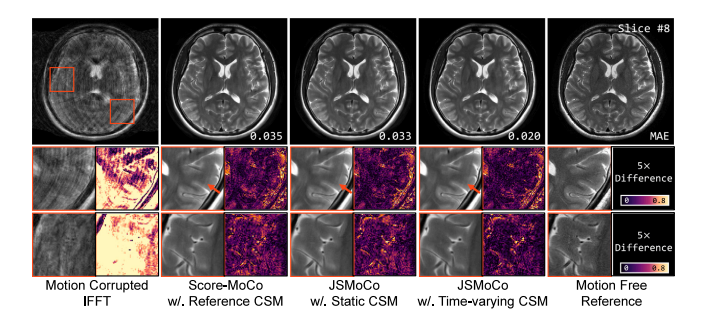
Fig. 9. Qualitative and quantitative comparisons of JSMoCo reconstructions using estimated static and time-varying coil sensitivity maps (CSMs) from motion-corrupted T2-weightedMRI data are presented. The mean absolute error (MAE) of each reconstructed image was calculated against the motion-free reference image. JSMoCo with estimated time-varyingCSMs achieves the lowest error, consistent with the differences shown in the zoomed-in regions. Compared to the other methods, the joint estimation of time-varying CSMseffectively reduces motion artifacts, as highlighted by the orange arrows
图9:展示了使用从受运动干扰的T2加权磁共振成像数据中估计的静态和时变线圈灵敏度图(CSMs),对JSMoCo重建结果进行的定性和定量比较。针对无运动的参考图像计算了每个重建图像的平均绝对误差(MAE)。使用估计的时变线圈灵敏度图的JSMoCo实现了最低的误差,这与放大区域中显示的差异一致。与其他方法相比,时变线圈灵敏度图的联合估计有效地减少了运动伪影,如橙色箭头所突出显示的那样。
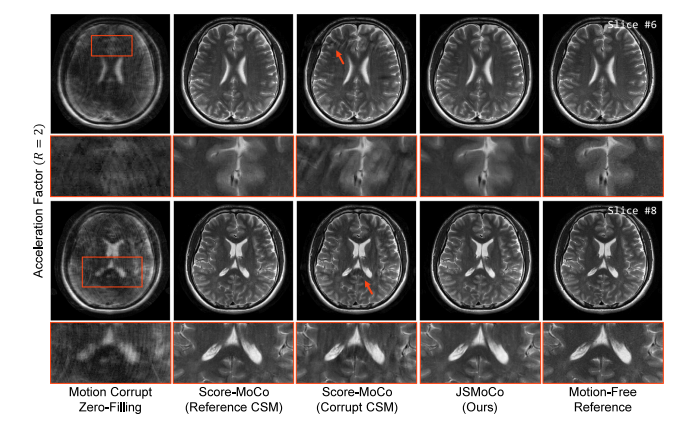
Fig. 10. Quantitative comparisons of reconstruction results for real-world motion-corrupted T2w human brain MRI scan with an acceleration factor of 𝑅 = 2.
图10:针对加速因子R = 2 的受真实运动干扰的T2加权人脑磁共振成像扫描的重建结果的定量比较
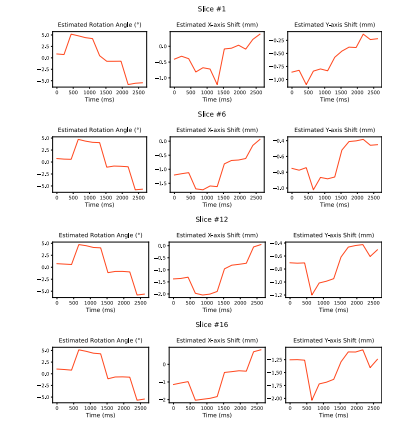
Fig. 11. Qualitative results of in-plane motion parameters estimation by JSMoCo onreal-world motion-corrupted T2w MRI data with an acceleration factor of 𝑅 = 2
图11:JSMoCo对加速因子R = 2 的真实运动干扰的T2加权磁共振成像(MRI)数据进行面内运动参数估计的定性结果。
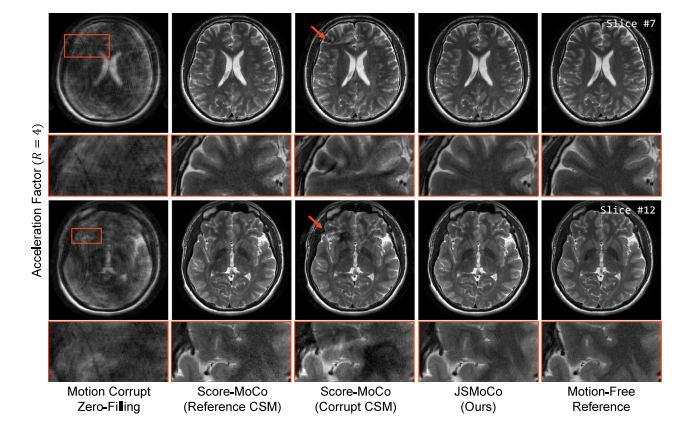
Fig. 12. Quantitative comparisons of reconstruction results for real-world motion-corrupted T2w human brain MRI scan with an acceleration factor of 𝑅 = 4.
图12:针对加速因子R = 4 的受真实运动干扰的T2加权人脑磁共振成像扫描的重建结果的定量比较。
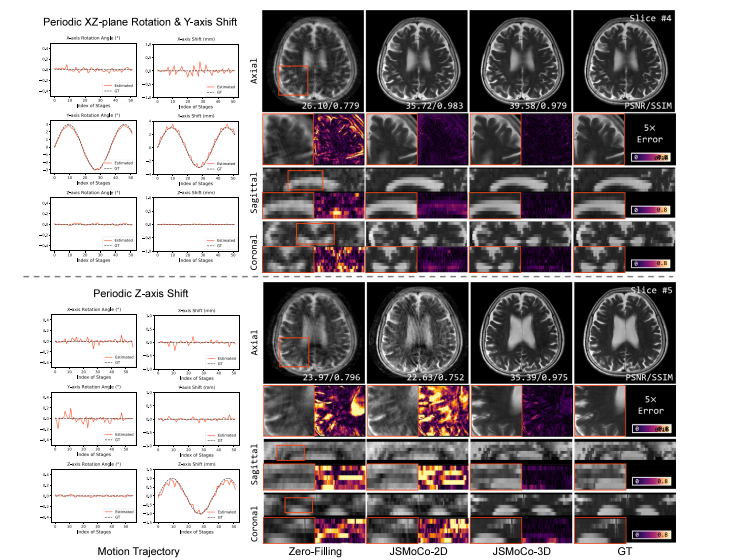
Fig. 13. Qualitative results of JSMoCo with 2D and 3D rigid transformation models, demonstrating performance under two simulated types of out-of-plane motion trajectories onthe fastMRI dataset. The left part of the figure shows the estimated motion parameters estimated by JSMoCo with the 3D motion forward model.
图13:采用二维和三维刚体变换模型的JSMoCo的定性结果,展示了在fastMRI数据集上两种模拟的面外运动轨迹下的性能。图的左侧部分显示了使用三维运动正向模型的JSMoCo所估计的运动参数。
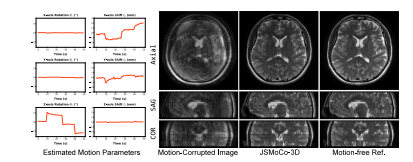
Fig. 14. Qualitative results of MRI image and estimated motion parameter by JSMoCo-3D on motion-corrupted in-vivo T2w data at an acceleration factor of 𝑅 = 2.
图14:JSMoCo - 3D在加速因子R = 2时,对受运动干扰的体内T2加权数据的磁共振成像(MRI)图像以及估计的运动参数的定性结果。
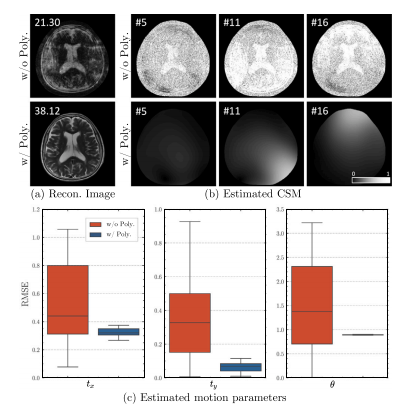
Fig. 15. Qualitative results for the reconstructed images and estimated CSMs, as well asquantitative results (PSNR) for estimated motion parameters with and without modelingCSM as a polynomial function.
图15:重建图像和估计的线圈灵敏度图(CSMs)的定性结果,以及将CSM建模为多项式函数和未将其建模为多项式函数时,估计的运动参数的定量结果(峰值信噪比(PSNR))。

Fig. 16. Reconstruction performance (PSNR and SSIM) with different acceleration ratesand different levels of motion.
图16:在不同加速率和不同运动水平下的重建性能(峰值信噪比(PSNR)和结构相似性指数(SSIM))。
Table
表

Table 1Meaning of mathematical notations in background and methods
表1 背景和方法中数学符号的含义
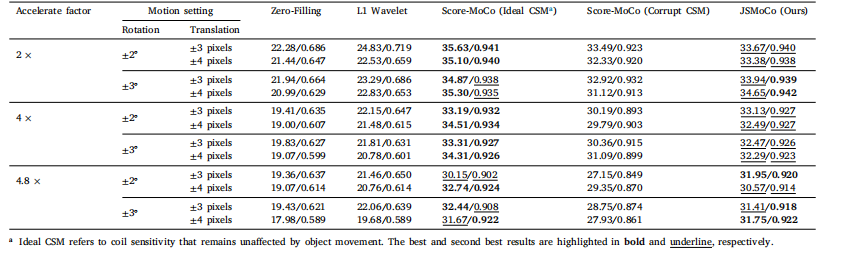
Table 2Quantitative results (PSNR/SSIM) of compared methods on the fastMRI dataset reconstruction with three acceleration factors (𝑅 = 2, 4, 4.8) and four motion parameters settings.
表2 在fastMRI数据集重建中,对比方法在三个加速因子(R = 2、4、4.8)和四种运动参数设置下的定量结果(峰值信噪比(PSNR)/结构相似性指数(SSIM))。
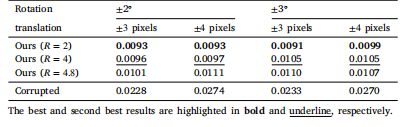
Table 3Quantitative results (NRMSE) of the estimated CSMs using the proposed method,compared with those obtained from motion-corrupted k-space signals using ESPIRiT,with reference to the ground truth CSMs.
表3:所提出的方法估计的线圈灵敏度图的定量结果(归一化均方根误差,NRMSE),与使用ESPIRiT从受运动干扰的k空间信号得到的结果相比,并以真实的线圈灵敏度图作为参考。
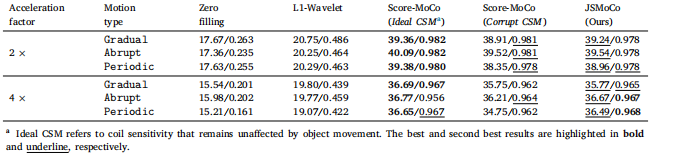
Table 4Quantitative results of JSMoCo when simulating different types of motion trajectory and different acceleration factor (2×, 4×) on the fastMRIT2 brain dataset (Knoll et al., 2020).
表4:在fastMRI T2脑部数据集(诺尔等人,2020年)上,JSMoCo在模拟不同类型的运动轨迹以及不同加速因子(2倍、4倍)时的定量结果。

Table 5Quantitative results of JSMoCo with 2D and 3D motion forward model when simulatingtwo types of out-of-plane motion on the fastMRI dataset. The best and second bestresults are highlighted in bold and underline, respectively
表5:在fastMRI数据集上模拟两种面外运动时,使用二维和三维运动正向模型的JSMoCo的定量结果。最优结果以粗体显示,次优结果加下划线标注。
