免疫细胞靶点“破局战”:从抗体到CAR-T,自免疾病治疗的3大技术突破
引言
人体免疫系统组成了一个严密调控的“网络”,时刻检测着外来病原体,并将其与自身抗原区分开来。但免疫系统也可能会被“策反”,错误的攻击我们自身,从而导致自身免疫性疾病的发生。
目前已知的自免疾病超过100种,如类风湿性关节炎、银屑病、多发性硬化症等。自免疾病的病因尚未完全明确,涉及多种免疫细胞,尤其是B细胞和T细胞。
越来越多的研究表明,B细胞在自免疾病中并非“单纯”的旁观者,而是积极的参与者。如今,靶向CD20、CD19、BAFF等蛋白的B细胞耗竭,已用于系统性红斑狼疮、多发性硬化症等。

义翘神州旨在为药物研发和生物标志物分析提供高质量的工具,推动自免疾病靶向开发和早期检测进展!
B细胞在自免疾病中的作用
B细胞和T细胞是适应性免疫的核心组成部分,在生物体的一生中,由骨髓中的造血干细胞祖细胞持续产生。
B细胞的主要功能是产生抗体。活化的B细胞在淋巴结和脾脏中分化为抗体分泌细胞(ASCs)。病理状态下,ASCs分泌的自身抗体通过调节信号通路、引发免疫复合物介导的炎症及消耗特定类型细胞,引发自免疾病。
B细胞在自免疾病生理学的多重作用,使其成为一系列自免疾病的靶点。B细胞可以产生多种影响自免疾病的细胞因子,如IL-6、TNF、IFNγ等。除CD20外,不同表面抗原,如CD19、BCMA、CD38、BAFF,在B细胞谱系的特定亚群表达。因此,B细胞在自免疾病发挥重要作用。
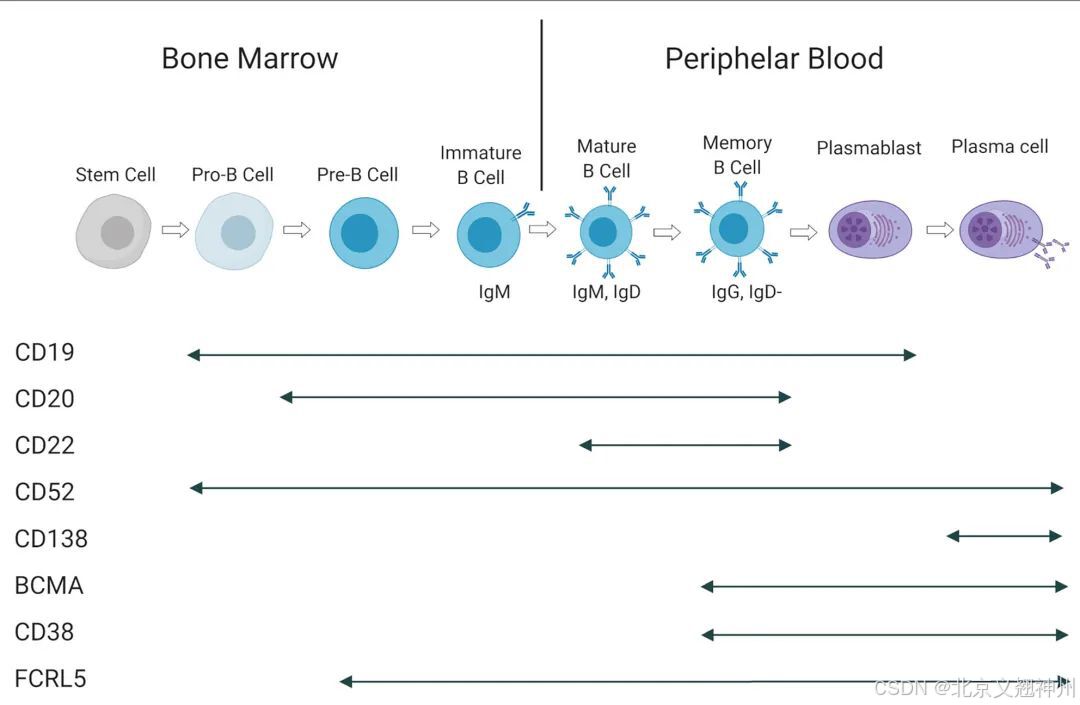
不同细胞表面抗原在不同B细胞谱系表达示意图(源自文献:doi: 10.3389/fimmu.2020.00762)
B细胞耗竭:撑起自免疾病“半边天”
通过B细胞机制来干预疾病的疗法统称为:B细胞耗竭疗法(BCDT)!
BCDT用于自免疾病治疗已有20多年的历史,始于杂交瘤技术制备单克隆抗体成为可能之时。1997年,首个抗CD20单抗利妥昔(Rituximab)获批上市,但直到2006年才首次获批用于类风湿性关节炎。
如今,多种B细胞耗竭药物已用于临床或正在开发中,如抗体药、CAR-T、TCE、ADC、小分子抑制剂等。
此外,抗CD38单抗靶向浆细胞,旨在改进和优化B细胞耗竭的治疗策略。
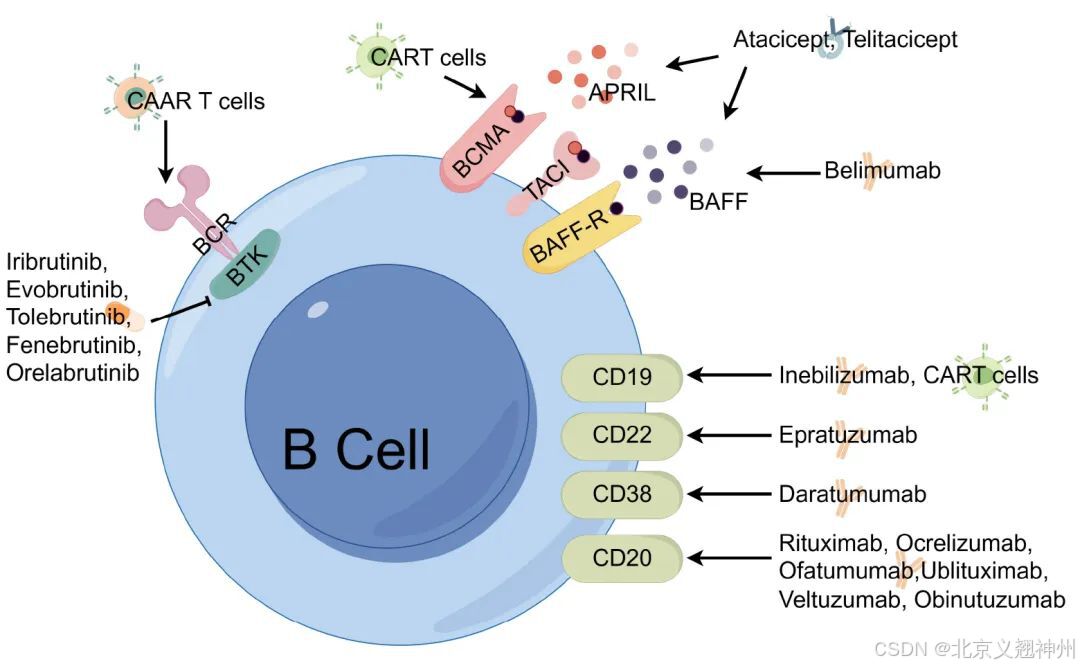
B细胞耗竭疗法(源自文献:doi: 10.3389/fimmu.2023.1322546)
接下来,我们将对单克隆抗体、双特异性抗体和CAR-T这3大类B细胞耗竭技术的研究进展进行介绍。
1、单克隆抗体抗体
与B细胞表面表达的抗原、配体或受体结合,抑制与细胞生长、增殖或凋亡机制相关的信号通路。比如抗体与CD20结合,使Ca2+浓度发生变化,进而控制B细胞的生长和凋亡。
除了通过抑制信号传导直接诱导靶细胞凋亡外,单抗可通过抗体依赖的细胞毒性(ADCC)、补体依赖的细胞毒性(CDC)、抗体依赖的细胞吞噬作用(ADCP)等间接清除靶细胞。
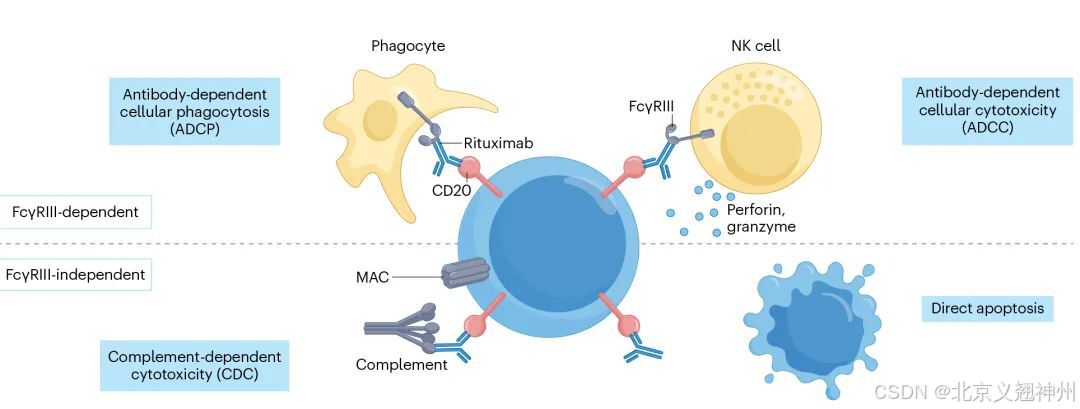
单抗耗竭B细胞的作用机制(以Rituximab为例,源自文献:doi: 10.1038/s41584-024-01210-9)
热门抗体研究进展!
CD20、CD19、CD22、CD38、BAFF
CD20
CD20几乎在B细胞发育的全过程均有表达,除前B细胞、浆母细胞和浆细胞阶段。靶向CD20的抗体应用最广泛,已被证明在多种自身免疫性疾病中都有活性。现有CD20单抗可分为Ⅰ型和Ⅱ型,Ⅰ型能使CD20易位或聚集到脂筏,Ⅱ型则不具备这种能力。
Ⅰ型抗体Rituximab属于嵌合鼠/人源单抗,已被批准用于多种自免疾病,如类风湿性关节炎、肉芽肿性多血管炎、寻常型天疱疮等。但其鼠源有时会引发免疫反应,因此人源化或全人源抗体应用潜力更大。新型靶向CD20的奥法妥木单抗(Ofatumumab)和奥瑞利珠单抗(Ocrelizumab)分别于2009年和2017年被FDA批准用于多发性硬化症。与Rituximab相比,Ofatumumab优化了CDC作用,而Ocrelizumab具有增强的ADCC作用。
Ⅱ型抗体可通过溶酶体介导的细胞死亡直接杀伤细胞。全人源化抗CD20奥滨尤妥珠单抗(Obinutuzumab)在Fc区的天冬酰胺297处进行糖基化改造,对FcγRIIIa的结合亲和力更高,增强ADCC作用,目前正在开展针对自免疾病的临床研究。另一款抗CD20单抗Ublituximab同样经过糖基化改造增强ADCC,已被批准用于复发型多发性硬化症。
CD19
人源化抗CD19单抗依奈利珠(Inebilizumab)已被FDA批准用于一种罕见的中枢神经系统自免疾病:视神经脊髓炎谱系障碍(NMOSD)。然而另一款CD19抗体在SLE患者中未达到临床试验终点。可能抗CD19单抗在自免疾病中的效果不如靶向CD19的CAR-T细胞吧。
CD22
依帕珠单抗(Epratuzumab)是靶向CD22的人源化单抗,抑制B细胞亚群的激活和分化,但B细胞数量不会显著减少。临床Ⅲ期试验结果显示Epratuzumab在系统性红斑狼疮(SLE)患者中效果良好。
CD38
CD38是B细胞尤其是浆细胞表面的重要生物标志物,具有细胞黏附、迁移及酶活性。CD38是原发性膜性肾病(PMN)、IgA肾病(IgAN)、SLE等自免疾病的潜力靶点。已获批上市的Daratumumab和Isatuximab正在积极拓展自免赛道,后来者Felzartamab和Mezagitamab正在进行临床研究。
BAFF
BAFF(也称为TNFSF13B、CD257)属于肿瘤坏死因子(TNF)配体家族成员,有可溶型和膜结合型两种形式。BAFF受体有3种:TNFRSF13B/TACI、TNFRSF17/BCMA、TNFRSF13C/BAFFR。通过与其受体的结合在B细胞的存活和增殖及自身免疫性B细胞的选择方面发挥关键作用。
目前,用于治疗SLE的有BAFF单抗贝利尤(Belimumab)和靶向BAFF和APRIL双靶点的融合蛋白类药物泰它西普(Telitacicept)。靶向BAFF-R的Ianalumumab单抗正在用于开发治疗SLE、干燥综合征等自免疾病。
2、双特异性抗体
双特异性抗体可通过同时识别和结合两种不同的抗原或抗原表位,提高疗效和安全性。T细胞衔接器(TCE)双抗在自免疾病领域备受关注,一方面是TCE双抗可以更直接有效的清除B细胞,另一方面则是更能满足自免疾病的临床需求。现阶段自免疾病主要围绕控制症状、减少炎症和延缓疾病进展为主,并不是完全清除所有的异常细胞,TCE双抗正好有这方面的优势。
已获批的B细胞耗竭TCE有靶向CD19xCD3的Blinatumomab,靶向CD20xCD3的Mosunetuzumab、Glofitamab、Epcoritamab等,用于白血病或淋巴瘤,自免疾病的研究尚处于临床阶段。
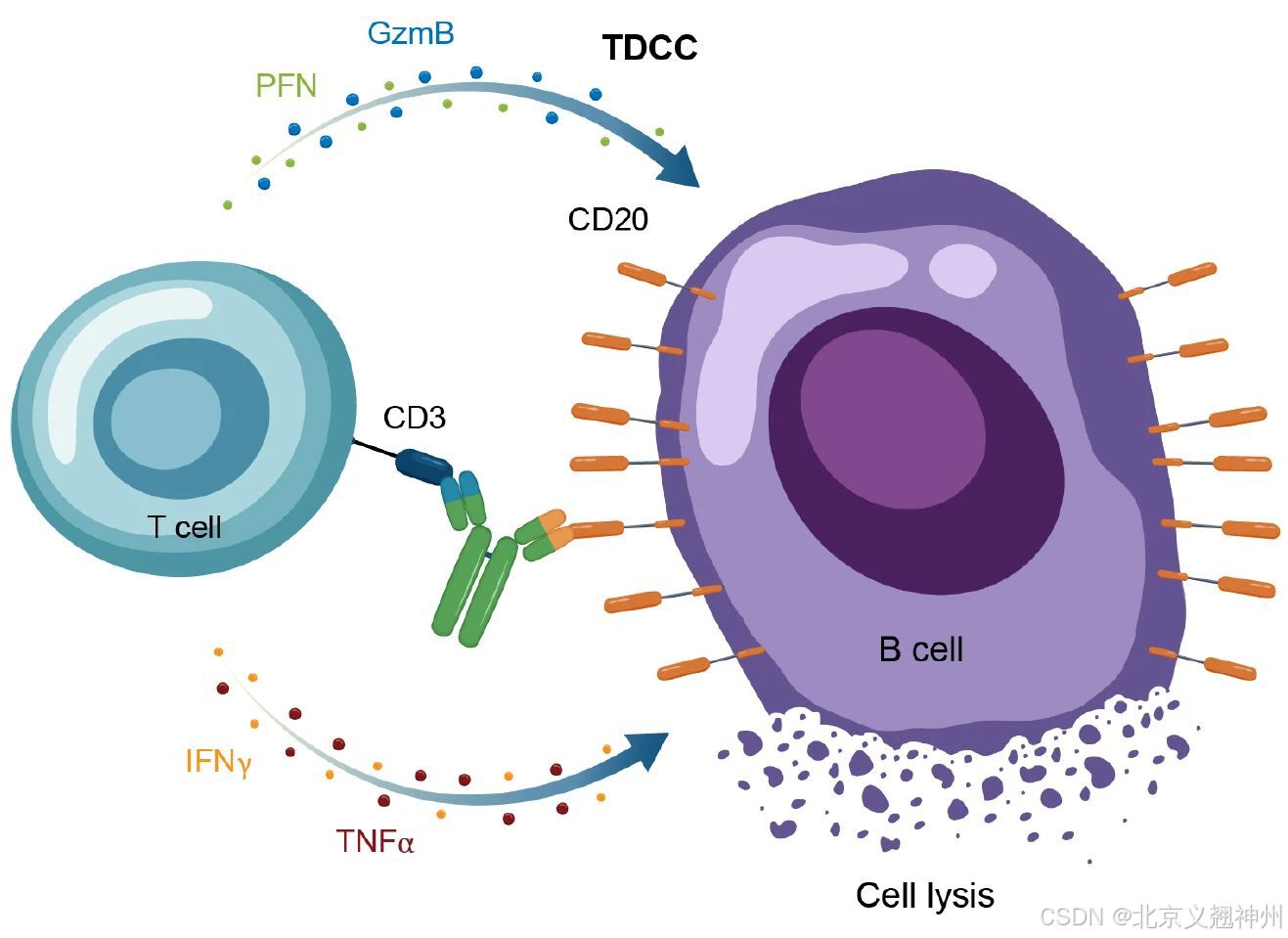
TCE作用机制(源自文献:doi: 10.3389/fimmu.2024.1454747)
3、CAR-T
以CD19为靶点的CAR-T已用于复发和/或难治性B细胞恶性肿瘤,在SLE和其他自免疾病中的应用已取得令人信服的早期结果。CAR-T用于自免的主要思路是消灭产生自身抗体的B细胞或浆细胞。
在CAR-T治疗中,CD19常用于B淋巴细胞瘤,BCMA用于多发性骨髓瘤,而在自免疾病中,这两个靶点均可以。研究发现与仅靶向CD19的CAR相比,同时靶向CD19和BCMA的双子CAR在自免领域可能更胜一筹。
目前有5款靶向CD19的CAR-T细胞疗法值得期待,分别为:
1. CD19 NEX-T
通过激活CAR-T细胞结构,释放炎症细胞因子和其他化学物质来破坏目标B细胞。用于治疗SLE,被BMS视为优先项目,希望“突破免疫介导疾病的新边界”。临床Ⅰ期结果显示3名随访至少6个月的SLE患者能够停止所有其他治疗,且没有出现新的疾病活动迹象。
2. CD19 KYV-101
清除功能失调的免疫细胞实现患者的“免疫重置”,独特之处在于其避免了细胞因子综合征,并提高耐受性。Kyverna正在进行僵人综合征(SPS)、重症肌无力和狼疮性肾炎3种疾病的临床研究,预计在2025年中期完成SPS的II期试验入组。
3. CD19 CTX112
“现货型”同种异体CAR-T,同时对TRAC、B2M、TGFBR2和ZC3H12A基因进行敲除以增强效力。CRISPR Therapeutics正在评估 CTX112 在多种自身免疫性疾病中的潜力,如系统性硬化症和炎症性肌病。
4. CD19 obe-cel
全称obecabtagene autoleucel,可实现快速抗原解离,无需REMS(风险评估缓解策略)。obe-cel已获得FDA批准,用于复发/难治性B细胞急性淋巴细胞白血病。Autolus正在开展用于治疗晚期SLE的Ⅰ期研究。
5. CD19 CABA-201
包含4-1BB结构域。Cabaletta正在评估其在多种自免疾病中的临床结果,如SLE、系统性硬化症、多发性硬化症、重症肌无力等。
总之,随着免疫系统研究的不断深入,恶性肿瘤与自身免疫性疾病之间的联系愈加紧密。利用肿瘤药物研发成果治疗自免疾病也富有成效,如近来CAR-T在自免领域的数据让我们看到深度B细胞耗竭疗法发潜力。未来还有望开发更多免疫细胞的靶点疗法。
✦义翘神州自免疾病研究解决方案✦
义翘神州提供全面的自身免疫性疾病解决方案,产品可用于近50种自免疾病的研究,包括靶点试剂,如靶点蛋白、细胞因子和激酶,同时还提供用于生物标志物研究的试剂。义翘神州旨在为药物研发提供和生物标志物分析提供高质量的工具,推动自免疾病靶向开发和早期检测进展。
免责声明:义翘神州内容团队仅是分享和解读公开的研究论文及其发现,专注于介绍全球生物医药研究新进展。本文仅作信息交流用,文中观点不代表义翘神州立场。随着对疾病机制研究的深入,新的实验结果或结论可能会修改或推翻文中的描述,还请大家理解。
本文不属于治疗方案推荐,如需获得治疗方案指导,请前往正规医院就诊。本司产品目前仅可用于科学研究,不可用于临床治疗。
【参考文献】
1. Lee, D.S.W., Rojas, O.L. & Gommerman, J.L. B cell depletion therapies in autoimmune disease: advances and mechanistic insights. Nat Rev Drug Discov, 2021. https://doi.org/10.1038/s41573-020-00092-2
2. Lejeune M, et al. Bispecific, T-Cell-Recruiting Antibodies in B-Cell Malignancies. Front. Immunol. 2020. doi: 10.3389/fimmu.2020.00762
3. Rui Li, et al. Editorial: Next generation B cell targeting therapies in autoimmune diseases. Front Immunol. 2023. doi: 10.3389/fimmu.2023.1322546
4. Stockfelt, M., et al. Opportunities and limitations of B cell depletion approaches in SLE. Nat Rev Rheumato, 2025. https://doi.org/10.1038/s41584-024-01210-9
5. William H. Robinson, et al. Cutting-edge approaches to B-cell depletion in autoimmune diseases. Front. Immunol., 2024, doi: 10.3389/fimmu.2024.1454747
